의인 크로이츠펠트-야코프병 예방을 위한 정책 제안: 골든 피어리드, 기구 추적 체계, RT-QuIC, 설계와 흡수 전략을 중심으로
A Policy Proposal to Prevent Iatrogenic Creutzfeldt-Jakob Disease: A Hybrid Framework of a Golden-Period Response, Instrument Tracking, RT-QuIC, and Design-and-Absorb Strategies
Article information
서 론
크로이츠펠트-야코프병(Creutzfeldt-Jakob disease, CJD)은 비정상 프리온(prion)에 의해 발생하며 빠르게 진행하는 치명적 신경퇴행질환이다[1-4]. 전 세계 크로이츠펠트-야코프병의 대다수는 산발성이지만 경막 이식, 뇌하수체유래성장호르몬, 각막 이식, 오염된 수술 기구, 혈액제제 등을 매개로 한 의인 크로이츠펠트-야코프병(iatrogenic CJD, iCJD)이 수십 년에 걸쳐 꾸준히 보고되었다[1-6]. 일본과 프랑스를 비롯한 여러 나라에서 특정 시기에 공급된 경막 이식재와 관련된 환자 집단이 확인되었고[2,3,6] 호르몬제제와 내시경, 수술 기구와 관련된 사례도 보고된 바 있다[1-5].
의인 크로이츠펠트-야코프병의 절대적인 발생 위험은 매우 낮다. 그러나 한 번 사고가 발생하면 잠복기가 수년에서 수십 년에 이르고 치명률이 사실상 100%이며 재사용 기구, 인체 유래물, 혈액제제를 통해 2차, 3차 전파 가능성이 열려 있다는 점에서 저확률 고영향(low probability, high impact) 위험에 해당한다[1-4]. 실제 사례에서는 수백에서 수천 명 규모의 역추적 조사(look-back), 대량 기구 폐기, 법적 비용, 언론 이슈, 의료기관 신뢰 상실이 뒤따랐다. 이러한 특성 때문에 의인 크로이츠펠트-야코프병은 개별 병원 차원을 넘어 국가 보건의료 체계의 신뢰와 지속 가능성에 영향을 미치는 위험으로 간주된다[1-6]. 이러한 위험을 줄이기 위하여 국제적으로는 의인성 전파 경로를 차단하기 위한 여러 수준의 정책과 지침이 축적되어 왔다. 세계보건기구(World Health organization, WHO), 질병통제예방센터(Centers for Disease Control and Prevention, CDC), 영국 위험병원체 자문위원회(Advisory Committee on Dangerous Pathogens, ACDP) 등은 조직 감염성에 따른 고위험, 저위험 조직 분류와 이에 따른 수술 기구 관리 원칙을 제시하고[7-13] 1 N NaOH 또는 2% 이상 차아염소산 1시간 침적 후 134℃ 18-60분 증기 멸균과 같은 강공정을 권고한다[7,8,11-13]. 영국과 유럽 일부 국가에서는 변형 크로이츠펠트-야코프병(variant CJD) 사태 이후 고위험 수술에서 일회용 기구 사용 확대, 고위험군에 대한 수술 전 위험도 문진 및 분류, 고위험 조직에 노출된 기구의 격리, 폐기, 장기 추적 감시 체계 등 보다 구체적인 운영 지침과 비용-효과 분석이 제시되어 왔다. 그 결과 수술 기구를 통한 2차 전파 위험을 체계적으로 낮추려는 국제적 노력은 이미 일정 수준으로 제도화되어 있다[1-4,7,8,11-13].
국내에서는 크로이츠펠트-야코프병이 「감염병의 예방 및 관리에 관한 법률」상 제3급 감염병으로 지정되어 있으며 의심, 확진 환자에 대한 신고 및 전수 감시, 역학 조사, 접촉자 관리 등이 국가 차원에서 이루어지고 있다[14,15]. 질병관리청은 프리온 질환 관리 지침 및 의료기관 감염관리 지침을 통해 의심 환자 평가, 인체 유래물이나 검체 취급, 부검 및 장기 조직 기증 제한, 고위험 수술 시 기본적인 소독 멸균 권고 사항을 제시하고 있다[14,15]. 그러나 이러한 지침은 주로 신고, 감시 및 일반적인 감염관리 원칙에 초점이 맞추어져 있어 실제 병원 현장에서 의인 크로이츠펠트-야코프병 위험을 최소화하기 위하여 어떤 시술에서, 어떤 기구를, 어느 시점까지, 어떤 강도의 공정으로 처리할 것인지를 시간축과 절차 관점에서 세분화한 현장 실행 매뉴얼은 아직 충분히 정교하게 마련되어 있지 않다[14,15].
특히 의심 및 확진 크로이츠펠트-야코프병 환자 수술 전후 시간축(0-60분, 24시간, 72시간, 72시간 이후)에 따른 단계별 조치, 기구 단위의 역추적 조사를 가능하게 하는 수술 기구 추적 관리 체계(instrument tracking system, ITS)를 활용한 정밀 역추적 조사 전략, 수술 전 및 수술 중 real-time quaking-induced conversion (RT-QuIC)을 이용한 고위험 환자 선별, 전용 세트, 특수 멸균, 일회용을 축으로 하는 설계와 흡수 전략처럼 국제적으로 논의되고 있는 요소들이 하나의 통합된 2차 예방 정책 모델로 정리되어 제시된 바는 거의 없다. 국내 의료기관은 각 병원 감염관리실과 진료과의 경험에 기반하여 개별적으로 대응해 왔으며 프리온 노출 사고 발생 시에도 기구 폐기, 역추적 조사 범위, 환자, 직원, 언론 소통에 있어 표준화된 의사결정 틀은 부족한 실정이다[5,6,14,15].
본 논문에서는 이러한 국제적 권고와 국내 제도 환경을 바탕으로 의인 크로이츠펠트-야코프병을 현실적으로 감당 가능한 범위 안에서 최대한 예방과 흡수할 수 있는 병원 내 2차 예방 정책 체계를 제시하고자 한다. 구체적으로 1) 크로이츠펠트-야코프병 노출 사고와 위험도 분류, 2) 골든 피어리드 3단계 모듈, 3) ITS 도입에 따른 정책 변화, 4) 고위험 수술 전 및 수술 중 RT-QuIC 선별 검사, 5) 설계와 흡수 전략(전용 세트, 특수 멸균, 일회용), 6) 구현 단계별 추진 계획과 핵심 성과 지표(key performance indicator, KPI)를 다룬다(Tables 1-5). 본 논문은 경제성은 2차적 고려로 두고 우선 임상적, 운영상으로 가능한 최선의 예방 체계를 제시한다는 전제를 바탕으로 하였으나 각 모듈과 전략에 대해 가능한 범위 내에서 비용 구조와 경제적 부담을 함께 서술함으로써 정책 결정자가 단계적 도입, 부분 적용, 우선순위 조정 등 재정 여건에 따른 재조정의 여지를 남기도록 설계하였다. 따라서 이 체계는 비용-효과성에 대한 최종 판단을 대신하기보다는 기존 WHO, ACDP, 질병관리청 지침과 양립하면서도 개별 병원이 의인 크로이츠펠트-야코프병 노출 사고를 체계적으로 관리하고 재발을 예방할 수 있도록 임상, 운영상 ‘어디까지 할 수 있는가’의 상한선을 제시하는 실질적 운영 모델을 제공하는 것을 목표로 한다.

Risk classification of exposure incidents in Creutzfeldt-Jakob disease (CJD) and recommended management of medical instruments

Three-phase classification of the Creutzfeldt-Jakob disease (CJD) response ‘golden period’ based on the Korean hospital system

Impact of implementing an instrument tracking system on the practical effectiveness of the Creutzfeldt-Jakob disease (CJD) response golden period

Comparison of prion decontamination and sterilization methods (illustrative cost example for one institution, not generalizable)
본 론
1. 크로이츠펠트-야코프병 노출 사고 정의와 위험도 분류
1) 크로이츠펠트-야코프병 노출 사고의 정의
본 논문에서 크로이츠펠트-야코프병 노출 사고란 다음 조건을 충족하는 상황을 의미한다: 1) 크로이츠펠트-야코프병 확진 또는 의심, 혹은 고위험 인자를 가진 환자의 2) 고감염 또는 잠재 감염 조직(뇌, 척수, 망막, 시신경, 경막, 편도, 림프절, 비장, 뇌척수액 등)에 노출된 수술 및 시술 기구, 조직, 체액이 3) WHO, CDC, ACDP가 권고하는 프리온 전용 비활성화 절차 없이 4) 다른 환자나 의료진에게 재사용되거나 접촉된 경우[7,8,11-13].
경막 이식, 각막 이식, 뇌하수체유래호르몬과 같이 인체 유래 제제도 광의의 노출 사고에 포함되며 특히 1980-90년대에 제조된 제제는 장기 보관된 재고나 과거 시술 이력 누락으로 인하여 현재도 잔여 위험이 존재할 수 있다[2-6].
골든 피어리드 기반 크로이츠펠트-야코프병 노출 사고 대응 모듈
1) 골든 피어리드의 개념과 크로이츠펠트-야코프병에의 적용
외상 영역에서 등장한 골든 피어리드는 치명적 손상이 비가역적으로 진행되기 전 적극적 처치로 예후를 바꿀 수 있는 한정된 시간창을 의미하며 이후 심정지, 뇌졸중, 패혈증 등 다양한 질환에서 시간 기반 목표가 설정되었다[16]. 크로이츠펠트-야코프병 노출 사고에서는 환자 생존 예후보다는 기구 오염 차단, 노출자 특정, 행정 비용 및 법적 비용 최소화가 목표이므로 다음과 같이 골든 피어리드를 재정의할 수 있다: 1) 0-60분: 건조 전 격리/습윤 유지 골든, 2) 60분-24시간: 추적-차단 골든, 3) 24-72시간: 소통 골든, 4) 72시간 이후: 사후 역추적 조사 단계. 각 단계별 핵심 조치는 Table 2에 요약하였다.
2) 0-60분: 건조 전 격리/습윤 유지 골든
프리온은 건조 후 표면에 강하게 고착되며 이 시점 이후에는 물리, 화학 세척 효율이 급격히 떨어진다[7-10]. 따라서 수술 종료 후 건조되기 전 60분은 기구를 습윤 상태로 유지 및 격리하고 추후 특수 멸균 또는 폐기 여부를 결정하기 위한 실질적 첫 골든 피어리드다. 정책적 최소 기준을 예시하면 다음과 같다. 수술 종료 후 5분 이내 허용된 point-of-use (POU) 효소폼/젤 또는 멸균수로 기구를 충분히 적시고 밀폐 가능한 습윤 컨테이너에 수납 후 세트 라벨에 환자 아이디, 수술 코드, 수술 번호, 종료 시각(T0), 조직 등급, CJD suspect 여부를 기록한다. 수술실에서 central sterile supply department (CSSD)로 이동 시 ITS 1차 스캔을 통해 전자 타임 스탬프를 생성한다. CJD suspect 세트임을 전화 및 전산으로 동시에 통보하고 CSSD 도착(T1), 세척 개시(T2) 시각을 자동 기록하며 T2-T0>60분일 경우 경보 발생 및 사유 코드를 입력한다. 이러한 standard operating procedure (SOP)는 프리온뿐 아니라 내시경 재처리 실패, 사람유두종바이러스(human papilloma virus, HPV), 칸디다 아우리스(Candida auris)와 같이 일반 소독에 저항성이 있는 기타 고위험 병원체 관리에도 긍정적인 부수 효과를 갖는다[9,10,17].
3) 60분-24시간: 추적-차단 골든
이 구간은 기구가 세척 및 멸균 공정에 진입하거나, 경우에 따라 이미 다른 수술에 사용되었을 수 있는 시간대이다. 핵심 정책 요소는 다음과 같다: 1) 기구 상태 확인 및 강공정 결정, 2) 세척 및 멸균 투입 여부, 배치 번호, 건조 여부 확인, 3) 고감염 조직 접촉 기구는 가능한 한 화학 소독(1 N NaOH 또는 2% 이상 NaOCl 1시간)에 추가하여 134℃ 18-60분 증기 멸균을 적용하거나 폐기 고려(Table 4) [7-10], 4) 로그 추적 및 환자군 특정, 5) operating room (OR), CSSD, 멸균기, ITS 로그와 전자의무기록을 교차 검증하여 동일 세트 사용 환자군을 특정하고 고/중/저위험군으로 분류(Table 1) [7,8,11-14], 6) 크로이츠펠트-야코프병은 국내에서 제3급 감염병으로 관리되고 있어 의심 및 확진 시 24시간 이내 질병관리청(Korea Disease Control and Prevention Agency, KDCA) 신고[11,14], 7) RT-QuIC, EEG, MRI, cerebrospinal fluid (CSF), 임상 소견 등 의심 근거를 포함해 신고하면 중앙 감시망과 연계되어 향후 역학 조사와 기술 지원을 받을 수 있다[14,15,18-23].
4) 24-72시간: 커뮤니케이션 골든
이 시기는 위험 소통(risk communication)의 관점에서 핵심이다. 72시간 이후로 노출자 통보가 미뤄지면 환자 및 보호자가 병원보다 먼저 외부를 통해 사실을 접할 가능성이 높아지고 불신, 소송, 언론 이슈가 증폭될 수 있다. 핵심 정책 요소는 다음과 같다: 1) 고위험군 환자에게는 전화 또는 대면 설명과 함께 크로이츠펠트-야코프병의 특성과 실제 추정 위험도, 추적 계획을 안내, 2) 저위험군에는 서면 안내문과 FAQ를 제공하여 과도한 불안을 피하면서도 알 권리 보장, 3) OR, CSSD, 관련 진료과, 행정부서에는 공통 Q&A를 배포하여 응답의 일관성 유지, 4) 병원 홍보팀, 법무팀과 협력하여 언론 및 온라인 대응 전략을 사전에 합의.
5) 72시간 이후: 사후 역추적 조사 단계
72시간 이후에 크로이츠펠트-야코프병 확진 또는 강한 의심이 제기된 경우, 이미 기구는 복수의 환자에게 재사용되었고 일부 로그는 소실 또는 덮어쓰기되었을 수 있다. 이 단계의 정책 목표는 가능한 범위 내에서 노출자와 기구를 최대한 특정하고 투명하고 일관된 커뮤니케이션으로 신뢰를 회복하며 근본 원인 분석을 통해 재발을 방지하는 것이다.
WHO 및 KDCA 기준에 따라 고/중/저위험군을 구분하고 통보 범위와 방식을 의료기관의 윤리위원회, 감염관리위원회, 법무팀, 홍보팀이 함께 결정하는 절차를 병원 규정으로 명문화하는 것이 바람직하다[11,12,14,15].
3. 수술 기구 추적 관리 체계와 데이터 기반 역추적 조사 정책
1) 수술 기구 추적 관리 체계의 개념과 구성요소
ITS는 의료기구에 부착된 바코드, 무선 주파수 식별(radiofrequency identification), 의료기기 고유 식별(unique device identification) 등을 통해 어떤 세트/기구가 어떤 수술에서 어떤 환자에게 어떤 순서로 사용되었는지를 실시간 또는 사후에 조회할 수 있는 체계이다[24-26]. 주요 구성 요소는 다음과 같다: 1) OR-CSSD-멸균기-병동/외래를 연결하는 통합 데이터베이스, 2) 세트/기구 ID, 환자 ID, 수술 코드, 시간, 담당자 정보, 3) POU 습윤 컨테이너 입출고 기록, 4) 특수 멸균 적용 여부, 폐기 여부, 역추적 조사 대상자 목록.
2) 수술 기구 추적 관리 체계가 골든 피어리드에 미치는 영향
ITS가 미비한 경우 시간 경과에 따라 기구 재사용 횟수가 증가하고 수기 기록에 오류가 쌓이며 로그가 삭제, 덮어쓰여 역추적 조사 정확도가 급격히 떨어진다. 반대로 ITS가 잘 구축된 경우 기구가 세척실로 이동하더라도 ID 태그를 통해 0-60분 내에 특정 및 격리가 가능하고 60분-24시간 구간에는 세척/멸균 배치와 환자군을 거의 100%에 가깝게 특정할 수 있으며 72시간 이후에도 백업 로그를 통해 상당 부분 역추적 조사가 가능하다[13-15]. 즉 ITS는 골든 피어리드의 물리적 시간 한계를 데이터 완결성 한계로 치환해 주며, 특히 사후 역추적 조사 단계에서 전량 폐기 대신 정밀 폐기, 정밀 역추적 조사를 가능하게 한다.
4. 고위험 수술 전 및 수술 중 RT-QuIC 선별 검사 정책
1) RT-QuIC의 진단 정확도와 국제 가이드라인
RT-QuIC는 미량의 PrPSc를 증폭하여 형광으로 검출하는 기법으로 다수의 연구와 메타 분석에서 크로이츠펠트-야코프병 진단에 있어 CSF 14-3-3과 총 타우(total tau)보다 우월한 민감도와 특이도를 보여준다[18-23]. 2세대 CSF RT-QuIC 연구에서는 민감도 92-96%, 특이도 98-100%가 보고되었다[18,21-23]. 여러 코호트 연구와 메타분석에서 산발 크로이츠펠트-야코프병 진단에서 RT-QuIC가 가장 정확한 생물표지자로 평가되었으며[18-23] 유럽과 미국의 최신 진단 가이드라인은 RT-QuIC 결과를 probable CJD 기준에 포함하고 있다[22,23]. 국내에서는 RTQuIC가 KDCA 의뢰 검사 항목으로 운영되며 임상에서는 공공 검사 형태로 진행되어 환자에게 별도 비용이 청구되지 않는다. 다만 결과 통보까지의 소요 시간은 검체 운송(주말·공휴일 포함) 및 검사실 운영 방식에 따라 변동될 수 있다. 따라서 결과가 확정되기 전이라도 본 논문의 골든 타임라인(특히 0-24시간)에서는 해당 기구를 즉시 격리 및 추적하여 재사용을 차단하고 결과 확인 후(양성/음성) 최종 처리한 뒤 이를 반영하여 관련 내용을 공유한다.
2) 고위험 수술 전 RT-QuIC 의무화 기준
모든 뇌, 척수, 후안부 수술에 일괄적으로 RT-QuIC를 시행하는 것은 비용, 시간, 침습성 면에서 비현실적이다. 따라서 수술, 임상, 병력 기준을 조합한 핵심 고위험군에 대해 선별 검사를 의무화하는 정책이 필요하다. 전자의무기록에서 수술 예약 시 A 고감염 조직(뇌, 척수, 후안부 등) 수술 예정, B 임상적으로 CJD 의심 또는 신경과 평가 필요 소견, C 병력/위험인자(과거 경막 이식, 뇌하수체 유래 제제 투여, 가족력 등)에서 A+(B 또는 C) 조건이 충족되면 팝업 창을 통해 RT-QuIC 미완료 경고와 함께 검사 주문 필드가 자동 활성화되도록 설계한다. 수술 전 외래 진료 및 입원에서 CSF 채취가 불가능한 경우 두개강 개방 직후 수술 중 CSF를 채취하여 RT-QuIC를 의뢰하는 수술 중 검사 루트(Fig.)를 병행한다. 국내에서 RT-QuIC 검사는 지정/공공 검사 체계를 통해 의뢰가 가능하나 검사 비용과 결과 통보까지의 소요 시간은 검체 운송(주말·공휴일 포함), 검사실 운영 및 배치 검사 여부 등에 따라 변동될 수 있다. 따라서 결과가 확정되기 전이라도 본 원고의 골든 타임라인(특히 0-24시간)에서는 해당 기구를 즉시 격리 및 추적하여 재사용을 차단하고 결과 확인 후(양성/음성) 기구를 최종 처리한 뒤 이를 반영하여 관련 내용을 공유하는 방식으로 운영한다.
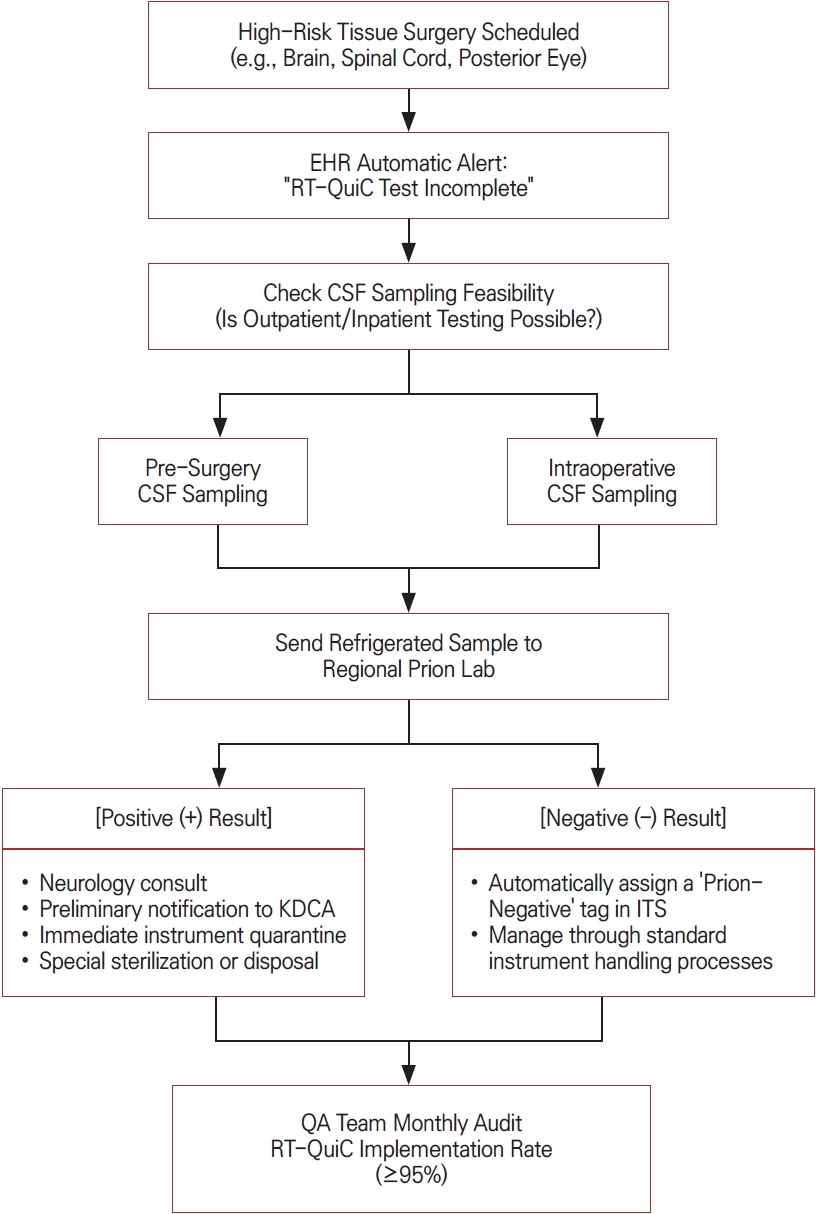
RT-QuIC screening and instrument-management workflow for high-risk tissue surgery. Arrows indicate the stepwise screening and instrument-management process. In surgeries involving high-infectivity tissues (e.g., brain, spinal cord, and retina), an EHR alert prompts RT-QuIC screening when testing has not been completed. CSF is obtained preoperatively when feasible or intraoperatively when preoperative sampling is not feasible, transported under refrigerated conditions to a regional prion laboratory, and followed by instrument management according to the RT-QuIC result. Positive results prompt immediate instrument sequestration and prion-specific decontamination or disposal, whereas negative results prompt prion-negative tagging in the ITS and standard reprocessing. Monthly QA audits monitor workflow completion, with a target of ≥95%. EHR; electronic health record, RT-QuIC, real-time quaking-induced conversion, CSF; cerebrospinal fluid, KDCA; Korea Disease Control and Prevention Agency, ITS; instrument tracking system, QA; quality assurance.
3) 1차·2차 예방 효과와 경제성
A+(B 또는 C) 고위험군이 전체 뇌, 척수 수술의 약 10%라고 가정하면 연간 1,200건 중(2차나 3차 병원을 가정하였을 때) 120건 정도에서 RT-QuIC가 추가 시행된다. RT-QuIC의 위음성이 5-10%라고 해도 강공정을 병행하면 잔여 위험은 크게 감소한다[18-21]. 반면 의인 크로이츠펠트-야코프병 역추적 조사, 폐기, 소송, 평판 비용은 1건당 수억 원 이상으로 추정되며[1-6,17,27] 연간 기대 사고 확률과 선별로 예방 가능한 비율을 고려하면 정책 차원에서 검토할 만한 비용-효과성을 가진다.
5. 설계와 흡수 전략: 전용 세트, 특수 멸균, 일회용
1) 탐지/사후 중심 전략의 구조적 한계
앞에서 설계한 골든 피어리드와 RT-QuIC는 탐지 및 사후에 속하는 전략이다. 그러나 1) 진단 지연: 위음성, turnaround time, RT-QuIC도 24-48시간의 검사 소요 시간과 위음성을 가진다[18-23]. 2) 운영상 복잡성: 선별-보고-수술 일정 조정-격리-특수 멸균-역추적 조사까지 많은 사람과 부서가 얽혀 있어 누락 및 지연 위험이 크다[7,8,12,13]. 3) 비용의 변동성: 넓은 범위의 선별은 검사비와 수술 지연비를 누적시키고 실제 사고는 극히 드물지만 발생 시 대형 비용을 초래한다[1-6]. 4) 사회적, 윤리적 부담: 광범위 선별은 낙인, 불안, 불필요한 수술 연기를 유발할 수 있다[11,12,14,15]. 이를 Table 5에서 정리한 탐지/사후 전략 vs. 설계와 흡수 전략과 비교하면 정책의 본축을 설계와 흡수에 두는 것이 더 구조적으로 안전하다는 점이 드러난다.
2) 프리온 특수 멸균 공정과 비용
여러 연구와 지침은 프리온 멸균에 대해 화학+고온 증기 멸균을 권장한다[7-10,15,28]. Table 4에서 보는 바와 같이 표준 멸균 공정(121℃ 15분)에 비해 프리온 멸균 비용은 +21%에서 +213% 수준으로 증가하지만 이는 의인 크로이츠펠트-야코프병 역추적 조사, 폐기, 법무, 평판 비용에 비하면 예측 가능한 소규모 보험료에 해당한다[1-4,6,17,27].
3) 전용 세트/일회용과의 조합
고감염 시술(뇌, 척수, 후안부)에 대해서는 전용 크로이츠펠트-야코프병 세트를 구성하여 의심 및 고위험 환자에서만이 아니라 원칙적으로 항상 강화 공정을 적용하도록 설계할 수 있다. 저가, 단순 구조, 후안부 접근 소모품은 일회용화를 통해 구조적 위험을 줄일 수 있다[6,9,24]. 영국의 편도·아데노이드 수술 일회용 기구 전면 도입 정책은 환자 선별보다 기구 변경을 통해 변종 크로이츠펠트-야코프병 2차 전파 위험을 흡수한 대표적 사례이다[27].
4) 설계와 흡수 중심 통합 운영 체계
본 논문에서 제시하는 운영 체계에서 설계와 흡수 전략은 상시 기본 안전선을 제공하고 RT-QuIC는 고위험 상황에서 강화 공정을 촉발하는 트리거, ITS는 노출자 특정과 역추적 조사 최소화, 골든 피어리드는 시간축상의 실행력을 확보하는 엔진으로 기능한다.
6. 구현 단계별 추진 계획과 KPI
1) 단계적 도입 추진 계획
(1) Phase 0 (즉시-1개월)
0-60분 습윤 유지 SOP를 수립하고 포스터, 포켓카드, 현장 교육을 실시한다. 저가 소모품(특히 후안부, 내시경 액세서리)의 일회용화를 확대한다. CJD suspect 라벨링, 로그 이중 백업 프로세스를 도입한다.
(2) Phase 1 (1-3개월)
신경외과, 안과(후안부), 두개저 수술용 전용 크로이츠펠트-야코프병 세트를 구성한다. 프리온 특수 멸균 알고리즘(Table 4)을 병원 표준으로 규정한다. 고감염 시술에서 전용 세트, 일회용 사용률을 80% 이상 달성할 수 있도록 한다.
(3) Phase 2 (3-6개월)
ITS 시범 도입 후 전 OR, CSSD, 멸균 공정으로 확대한다. 수술 예약 시 A+(B 또는 C) 조건에 따라 RT-QuIC 팝업, 자동 주문 기능을 구현한다(Table 3). 골든 피어리드(0-60분, 24시간, 72시간) 대응 프로토콜을 감염관리위원회 규정에 편입한다.
(4) Phase 3 (6-12개월)
다음의 항목에 대하여 KPI 모니터링을 수행한다: 고감염 시술 전용 세트 사용률 ≥95%, 프리온 특수 공정 준수율(농도, 온도, 시간) ≥98%, ITS 추적 완결성 ≥99%, RT-QuIC 고위험군 적용률 ≥95%, 크로이츠펠트-야코프병 노출 사고 발생 시 72시간 내 소통 완료율 ≥95%.
2) Neurology policy 관점에서의 정책 권고
Neurology policy section의 관점에서 본 논문이 제안하는 정책 메시지는 다음과 같이 요약할 수 있다.
첫째, 선별 중심이 아닌 설계 중심이 되어야 한다. 크로이츠펠트-야코프병은 잠복기, 위음성, 진단 지연으로 인하여 선별만으로는 안전을 보장할 수 없다. 따라서 고감염 시술 자체를 전용 세트, 특수 멸균, 일회용으로 설계해야 한다.
둘째, ITS와 데이터 기반 거버넌스를 도입해야 한다. ITS 도입은 의인 크로이츠펠트-야코프병뿐 아니라 내시경 재처리, HCV, HPV 등 광범위한 감염 관리에서 새로운 표준이 된다[24-28].
셋째, 골든 피어리드를 수립하고 윤리적 소통을 수행해야 한다. 0-60분, 24시간, 72시간이라는 시간축을 정책에 명시하고 환자, 직원, 언론과의 투명한 소통을 제도화해야 한다.
넷째, 국가 감시 체계와의 연계가 필요하다. KDCA 지침[11,14,15]과 병원 내부 정책을 정합적으로 설계하여 사고 발생 시 병원과 국가가 같은 언어로 대응할 수 있어야 한다.
결 론
의인 크로이츠펠트-야코프병은 거의 일어나지 않지만, 한 번 일어나면 너무 큰 사건이다. 프리온의 특성상 절대적 제로 리스크는 불가능하나 고감염 시술의 설계와 흡수(전용 세트, 특수 멸균, 일회용), 골든 피어리드(0–60분, 24시간, 72시간) 기반 신속 대응, 수술기구 추적 관리 체계를 통한 정밀 역추적 조사와 기구 관리, RT-QuIC을 활용한 표적 선별을 결합한 통합 정책 운영 체계는 국내 의료기관에서 의인 크로이츠펠트-야코프병 위험을 현실적으로 거의 발생하지 않는 수준까지 낮출 수 있는, 현실적인 단계별 추진 계획이다. 신경과, 신경외과, 감염관리, 중앙공급실, 정책 당국이 함께 이 운영 체계를 논의하고 병원 규모와 자원에 맞게 조정 및 도입한다면 크로이츠펠트-야코프병 뿐 아니라 향후 등장할 수 있는 프리온급 고위험 병원체, 복잡 내시경 감염, HPV, Candida auris 등의 위험까지 흡수할 수 있는 장기적 감염 관리 인프라를 구축하는 계기가 될 것이다.
Notes
ACKNOWLEDGEMENTS
본 연구는 질병관리청의 용역 과제로 수행되었으며 연구 수행이 가능하도록 지원해 주신 관계자 여러분께 깊이 감사드린다. 특히 프리온 질환의 감염 관리 및 의료기기 재처리 현장과 관련하여 자문과 협조를 제공해 주신 감염관리실, 중앙공급실(CSSD), 수술실, 검사실 및 관련 임상과 의료진과 실무 담당자들께 감사드린다. 또한 국내 지침과 현장 적용 가능성을 종합하는 과정에서 유익한 의견을 나누어 주신 공중보건 및 정책 담당자, 연구 준비와 문서화에 도움을 주신 모든 분들께 감사의 뜻을 전한다.
