| J Korean Neurol Assoc > Volume 39(3); 2021 > Article |
|
Abstract
Neuroleptic malignant syndrome (NMS) is a life-threatening neurologic emergency associated with the use of dopamine receptor-antagonist properties or the rapid withdrawal of dopaminergic medications. NMS is characterized by refractory hyperpyrexia, altered mental state, dysautonomia, and rigor. If hyperpyrexia persists, it can result in multiorgan failure. Herein, we report a case of NMS occurring after metoclopramide administration in a patient with pontine hemorrhage, which was successfully treated with targeted temperature management using a surface cooling device.
신경이완제악성증후군(neuroleptic malignant syndrome)은 도파민 수용체 길항제 사용 또는 도파민 약물의 급속한 중단으로 인해 발생하는 5-20%의 사망률을 가지는 신경계 응급질환이다[1]. 신경이완제악성증후군은 고열, 경축, 자율신경장애, 의식저하의 증상을 일으키며 횡문근융해, 급성호흡곤란증후군 및 파종혈관내응고 뿐만 아니라 급성 신부전 및 급성 간부전을 포함한 다기관 기능장애를 유발할 수 있다[1,2]. 신경이완제악성증후군은 도파민-2 수용체 차단으로 시상하부의 온도 설정 값이 올라가고 열 방출 기전이 손상되기 때문에 해열제에 불응하는 고열이 특징적으로 나타난다[2]. 지속적인 고열이 조직의 저산소증과 쇼크를 유발하여 다기관 부전이 발생하므로 신경이완제악성증후군에서의 고열을 즉각적이고 적극적으로 해결해야 환자의 예후를 호전시킬 수 있다[2,3]. 저자들은 다리뇌 출혈 환자에게 메토클로프라마이드(metoclopramide)를 다회 투약한 이후 발생한 신경이완제악성증후군에 대해 표면냉각장치(surface cooling device)를 이용한 목표체온유지 치료(targeted temperature management)를 적용하여 성공적으로 치료한 증례를 경험하였기에 이를 보고한다.
이전 특이 병력이 없던 36세 남자가 갑자기 발생한 의식 변화로 응급실에 왔다. 신경계진찰에서 동공의 크기는 양측 모두 2 mm였으며, 동공반사는 양측에서 소실되었다. 각막반사와 눈머리반사가 소실되었으며 사지 모두 통증에 반응하지 않았고 바뱅스키반사는 양측 모두 폄근발바닥반응(extensor plantar response)을 보였다. 뇌 컴퓨터단층촬영(computed tomography, CT)에서 다리뇌 출혈(pontine hemorrhage) 및 폐쇄수두증(obstructive hydrocephalus)이 진단되었고, 응급 뇌실외배액(external ventricular drainage)을 시행한 후 뇌신경계 중환자실로 입원하였다(Fig. 1). 뇌실외배액 시행 3시간 뒤 동공 크기는 양측 모두 2 mm로 변화가 없었으나 동공반사는 정상으로 회복되었다. 의식은 반혼수(semicoma)로 지속되었고 혈압 조절 및 인공호흡기 치료를 시행하였다. 입원 8일째 경피적확장기관절개술(percutaneous dilatational tracheostomy)을 시행하였으며 입원 15일째 발열 없이 활력징후가 양호해져 중환자실에서 뇌졸중 집중치료실로 전실하였다.
입원 14일째 딸꾹질이 시작되었고 바클로펜(baclofen)을 5 mg tid로 투약하였으나 호전 없이 지속되어 입원 15일째 메토클로프라마이드 10 mg을 정맥으로 투약하기 시작하였다. 입원 16일째 38.5℃의 발열을 보였고, 입원 18일째 40.9°C까지 체온이 상승하면서 혈압 73/41 mmHg, 호흡 30회/분, 맥박 130회/분으로 저혈압, 빈맥, 빈호흡이 발생하였고 무뇨, 경축이 동반되었으며 혈액요소질소 65 mg/dL, 크레아티닌 3.43 mg/dL, 크레아틴인산화효소(creatine phosphokinase) 3,200 IU/L 이상으로 확인되었다. 환자의 발열은 반복적인 해열제 투약에도 호전 없이 40°C 이상으로 지속되었고, 생리식염수 1 L 투여와 노르에피네프린(norepinephrine)을 32 μg/min까지 투약하였음에도 쇼크 상태가 지속되었다. 갑자기 발생한 고열의 원인을 감별하기 위해 혈액검사, 혈액, 소변, 가래에 대한 세균배양검사 및 가슴 X선, 뇌 CT를 촬영하였다. 혈액검사에서 백혈구 19,760/mm3, C-반응단백질 3.52 mg/L로 상승 소견을 보였지만 이는 전일 시행한 결과보다는 감소된 결과였고, 세균배양검사에서 동정된 균은 없었으며, 가슴 X선에서 폐렴 소견은 없었고, 설사, 피부 발진 등 감염 의심 소견도 없었다. 뇌 CT에서 혈종 확장이나 부종 증가의 소견은 없었고 수두증도 호전된 상태였다. 메토클로프라마이드를 투약하기 시작한 이후부터 고열이 시작된 점과 투약이 반복될수록 악화되는 양상(Fig. 2-A)을 고려하여 메토클로프라마이드 투약으로 인한 신경이완제악성증후군으로 추정 진단하였다. 이에 메토클로프라마이드 투약을 즉시 중단하였으며 신경계 중환자실로 전실하여 저온생리식 염수(cold saline) 1 L 투여 및 37°C 체온을 목표로 표면냉각장치를 적용하여 목표체온유지 치료를 시작하였다. 표면냉각장치를 부착한 시점에서 유치 도뇨관 체온계로 측정한 중심 체온은 39.6°C였고 4시간반만에 37°C에 도달하였고(Fig. 2-A) 빈맥, 빈호흡, 무뇨, 강직이 6시간 내에 모두 호전되었으며, 19시간 만에 노르에피네프린 투약을 종료하였다(Fig. 2-B). 목표체온유지 치료를 시작한 시점에서의 혈청 크레아티닌은 3.43 mg/dL였으며 48시간 후 정상 범위로 호전되었다. 또한 12,000 IU/L 이상으로 확인되었던 혈청 크레아틴인 산화효소도 1주일 뒤에 644 IU/L로 호전되었다(Table). 총 112시간 동안 목표체온유지 치료를 적용하였고 종료 후 체온은 37°C로 유지되었다. 목표체온유지 치료를 종료한 시점에서 신경이완제악성증후군에 의해 발생한 다기관 부전은 모두 회복되었고, 안정적으로 생체징후가 유지되어 일반병실로 전실하였다. 이후 다리뇌 출혈로 인한 반혼수 상태는 지속하였지만 신경이완제악성증후군으로 인해 발생한 다기관 부전은 호전된 상태로 유지되었으며, 딸꾹질에 대해서는 가바펜틴(gabapentin) 100 mg tid로 조절하였다. 환자는 보존적 치료를 위해 타원으로 전원되었다.
본 증례의 다리뇌 출혈 환자는 메토클로프라마이드 다회 투약 이후 이상 고열 및 쇼크를 동반한 신경이완제악성증후군이 발생하였고, 목표체온유지 치료를 적용함으로써 발열을 신속하게 조절하여 증세의 악화를 막고 다기관 부전에서 회복될 수 있었다.
신경이완제악성증후군은 5-20%의 높은 사망률을 보이는 신경계 응급상황으로 빠른 진단과 즉각적인 치료 개입이 예후를 호전시키는 데 매우 중요하다[1]. 본 증례와 같이 심한 다리뇌 출혈 환자에서 고열이 발생한 경우 감염, 중추성 발열, 발작교감과활성증, 신경이완제악성증후군, 세로토닌증후군 등을 빠르게 감별하여야 한다[2,4]. 발진 여부 확인 등의 신체진찰, 혈액검사, 세균배양검사 및 영상검사 등을 통해 감염병터를 확인하는 것이 중요하며, 감염원에 대한 증거가 없을 때 중추성 발열을 고려해볼 수 있다. 다리뇌출혈 후 중추성 발열은 비교적 초기부터 발생한 뒤 지속되는 특징이 있으며 본 증례처럼 초기에는 없었던 고열이 갑자기 발생한 경우 뇌 CT를 통해 다리뇌 출혈 악화 여부를 확인하여야 한다. 또한, 발열과 함께 혈압, 맥박의 심한 변화, 즉 자율신경계장애가 발작적으로 나타난다면 발작교감과활성증을 고려해볼 수 있다[4]. 발열 전에 새롭게 투약을 시작한 약제에 대한 조사가 중요하며 약제 투약 시점과 발열 악화 시점의 시간적 선후 관계가 뚜렷하게 보인다면 약물로 인한 고열 가능성을 확인하여야 한다. 본 증례의 경우 갑자기 발생한 고열과 이어서 발생한 쇼크 상태의 원인에 대해 감염의 증거는 확인되지 않았고, 추가로 시행한 뇌 CT에서 재출혈 소견이 없었으며, 투약력을 조사하였을 때 메토클로프라마이드가 투약되기 시작한 후부터 발열이 시작되었고 투약을 반복할 때마다 발열이 악화되었기 때문에 신경이완제악성증후군의 가능성이 가장 높다고 판단하였다. 본 환자에서는 심한 다리뇌 출혈로 인해 뇌간의 도파민 경로 등이 손상되었기 때문에, 메토클로프라마이드에 의한 신경이완제악성증후군 발병이 보다 쉽게 유발되었을 가능성을 고려하였다. 그러므로 심각한 뇌간 손상을 동반하는 다리뇌 출혈 환자에서 딸꾹질이나 구토에 대한 약물 치료 시 신경이완제악성증후군을 유발할 수 있는 약물을 선택할 경우 주의가 필요하며, 약물 투약 후 환자의 증상 변화를 면밀히 관찰할 필요가 있다고 저자들은 생각한다.
신경이완제악성증후군에서는 해열제에 불응하는 고열로 인해 대사 및 산소 요구량이 증가되어 일반적으로 심박출량이 증가되는데[3,5] 보통 체온 1°C 상승 시 산소 요구량이 10% 증가하게 된다[6]. 따라서 지속적인 고열은 조직의 저산소증과 쇼크를 유발하고 결국 다기관 부전이 발생한다[3,5]. 그러나 신경이완제악성증후군에서의 고열은 해열제나 수동냉각방법(manual cooling method)에 반응하지 않는 경우가 많으므로 목표체온유지 치료를 적용하는 것이 효 과적일 수 있다[3,7-9]. 목표체온유지 치료는 크게 침습방식과 비침습 방식으로 나뉘며, 침습방식은 혈관내 냉각방법으로 풍선(balloon)이 있는 열교환도관을 대퇴 정맥에 삽입하고 이를 외부 온도제어 장치에 연결하여 닫힌 순환경로를 형성한 뒤 이 경로를 통해 목표 체온에 도달하기 위한 냉각된 생리식염수가 혈관 내와 체외의 온도제어 장치를 순환하는 방법이며, 표면냉각장치를 사용한 비침습 방식은 가슴과 허벅지에 젤 패드를 부착하고 패드에 목표체온에 도달하기 위한 적절한 온도의 물을 주입시켜 체온을 조절하는 방법이다[10]. 본 증례에서는 치료가 필요한 시점에서 빠르고 쉽게 적용이 가능한 표면냉각장치를 사용한 비침습방식을 선택하였고 해열제에 반응하지 않는 고열을 4.5시간만에 해결함으로써 다기관 부전으로부터 비가역적인 손상 없이 회복될 수 있었다. 신경이완제악성증후군에 목표체온유지 치료를 적용한 증례가 외국에서 보고된 바 있지만[7-9], 대부분 침습적 방식을 사용한 경우이며 표면냉각장치를 이용한 목표체온유지 치료를 적용하여 치료한 증례[3]는 매우 드물며, 국내에서는 저자들이 아는 한 보고된 바 없다. 이에 본 증례를 통해 신경이완제악성증후군에 대한 효과적인 치료로써 표면냉각장치를 이용한 목표체온유지 치료를 제안하며 더불어 추후 신경이완제악성증후군과 유사하게 해열제에 반응이 떨어지는 고열이 동반되는 악성고열(malignant hyperthemia), 악성긴장증(malignant catatonia) 등의 질환에 대해서도 목표체온유지 치료 적용의 가능성을 제시하는 바이다.
REFERENCES
1. Oruch R, Pryme IF, Engelsen BA, Lund A. Neuroleptic malignant syndrome: an easily overlooked neurologic emergency. Neuropsychiatr Dis Treat 2017;13:161-175.



2. Berman BD. Neuroleptic malignant syndrome: a review for neurohospitalists. Neurohospitalist 2011;1:41-47.


3. Storm C, Gebker R, Kruger A, Nibbe L, Schefold JC, Martens F, et al. A rare case of neuroleptic malignant syndrome presenting with serious hyperthermia treated with a non-invasive cooling device: a case report. J Med Case Rep 2009;3:6170.



4. Ko SB. Paroxysmal sympathetic hyperactivity in the neurological intensive care unit. J Neurocrit Care 2015;8:66-72.

5. Suwanwongse K, Shabarek N. Hyperpyrexia in patients with COVID-19. J Med Virol 2020;92:2857-2862.


6. Jeong HG, Lee Y, Song KH, Hwang IC, Kim ES, Cho YJ. Therapeutic temperature modulation for a critically ill patient with COVID-19. J Korean Med Sci 2020;35:e210.

7. Dijkstra A, Knook AHM, Epker JL, Bakker J. Endovascular cooling for neuroleptic malignant sydrome; a case report. Neth J Crit Care 2010;15:81-83.
8. Diedler J, Mellado P, Veltkamp R. Endovascular cooling in a patient with neuroleptic malignant syndrome. J Neurol Sci 2008;264:163-165.


Figure 1.
Brain computed tomography shows a pontine hemorrhage with extension to 4th ventricle and mild hydrocephalus.
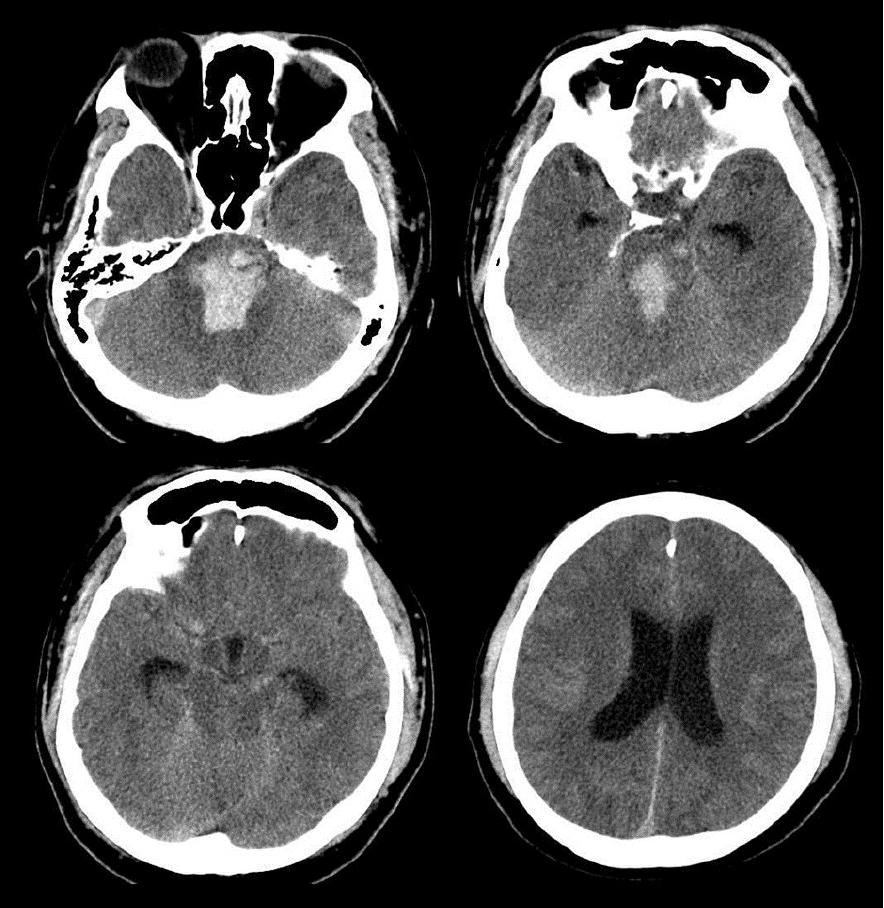
Figure 2.
(A) Changes in body temperature before and after applying TTM, metoclopramide injection time and water temperature of the surface cooling device. From an initial core temperature of 39.6°C, the target temperature was attained within 4.5 hours. (B) Changes in heart rate, mean arterial blood pressure and norepinephrine requirement before and after applying TTM. TTM; targeted temperature management.
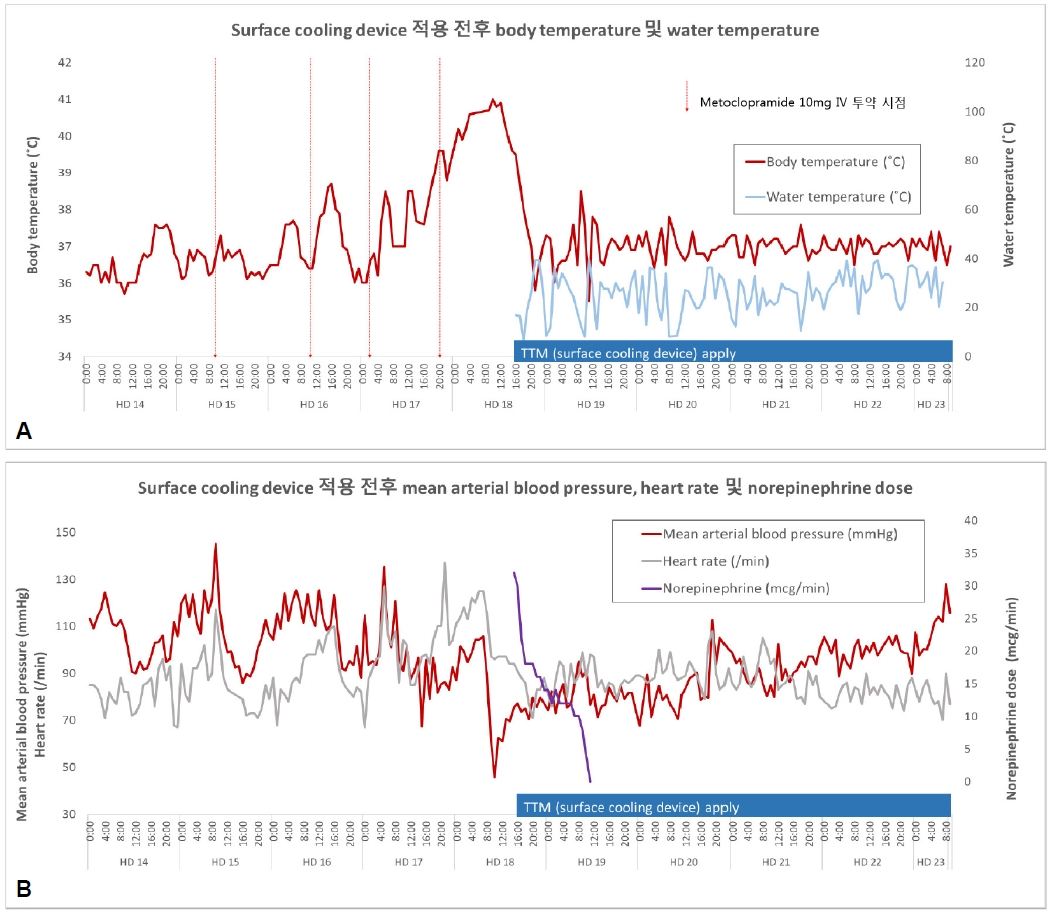
Table.
Changes in serial laboratory test results after applying TTM
- TOOLS
-
METRICS

-
- 0 Crossref
- 0 Scopus
- 1,544 View
- 57 Download
- Related articles
-
Progressive Moyamoya Syndrome Associated with Paroxysmal Nocturnal Hemoglobinuria2014 ;32(4)
Neuroleptic Malignant Syndrome Caused by Long Term Intake of Haloperidol2011 ;29(3)
Churg-Strauss Syndrome Complicated With Intracerebral Hemorrhage2009 ;27(3)



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print