양측 경동맥스텐트삽입술 시행 후 발생한 후대뇌동맥 영역 뇌경색
Posterior Cerebral Artery Territory Infarction after Bilateral Carotid Artery Stenting
Article information
Trans Abstract
Carotid artery stenting (CAS) is considered for patients with symptomatic carotid stenosis of 50% or greater. Following CAS, hemodynamic changes can alter the cerebral perfusion status. Furthermore, hypotension and bradycardia may occur due to the stimulation of carotid sinus baroreceptors. A more meticulous approach to these hemodynamic changes is required, especially in patients with bilateral carotid artery stenosis and concurrent multiple cerebrovascular stenoses. This report presents a case of posterior cerebral artery territory infarction that occurred after bilateral CAS.
유증상 경동맥협착 환자의 경우 50% 이상의 협착이 확인되면 경동맥스텐트삽입술 시행을 고려할 수 있다[1]. 경동맥스텐트삽입 이후 혈역학 변화로 인하여 뇌관류 상태가 변할 수 있으며 경부 압력수용체 자극에 의한 저혈압 및 서맥 등의 증상이 발생할 수 있다[2]. 특히 양측 경동맥협착을 포함한 다발성 뇌혈관협착 환자에서는 이러한 혈역학 변화에 대한 보다 세심한 접근이 필요하다. 본 증례는 양측 경동맥스텐트삽입술 시행 후 후대뇌동맥(posterior cerebral artery, PCA) 영역의 경색이 발생한 사례로, 그 진단 및 치료 과정을 보고하고자 한다.
증 례
고혈압, 당뇨병, 고지혈증의 기저 질환이 있는 70세 남자가 4주 전 발생한 일시적 좌측 위약을 주소로 내원하였다. 현장에서 작업 중 발생한 좌측 위약은 약 2-3분간 지속 후 호전되었다. 타원에서 시행한 뇌자기공명영상(magnetic resonance imaging, MRI) 및 컴퓨터단층혈관조영술(computed tomography angiography, CTA)에서 양측 근위부 경동맥의 심한 협착이 확인되었다. 외래에서 아스피린(aspirin)과 클로피도그렐(clopidogrel)을 이용한 이중항혈소판제 치료를 시작하였으며 약 2개월 반 동안 투약을 유지한 뒤 경동맥스텐트삽입술 시행을 위하여 입원하였다.
입원 3일 전부터 좌안 시력 저하가 발생하였고 입원 당시 좌측 상하지 감각 저하 및 경미한 좌측 안면마비가 관찰되었다. 입원 당일 시행한 뇌MRI의 확산강조영상(diffusion-weighted imaging)에서 우측 중대뇌동맥 경계부, 우측 피질, 좌측 전두엽 및 두정엽 부위에 다발성 고신호강도 병변이 관찰되었다. CTA에서는 양측 근위부 경동맥의 심한 협착과 함께 우측 원위부 경동맥의 미만성(diffuse) 협착이 확인되었다. 양측 척추동맥(vertebral artery) 및 기저동맥(basilar artery)에는 유의한 협착이 없었으나 좌측 PCA 제2분절 부위에 심한 협착이 관찰되었다(Fig. 1). 대퇴동맥경유뇌혈관조영술(trans femoral cerebral angiography)에서 우측 근위부 내경동맥은 North American Symptomatic Carotid Endarterectomy Trial (NASCET) 기준 91%, 좌측 근위부 내경동맥은 82% 협착이 확인되었다.
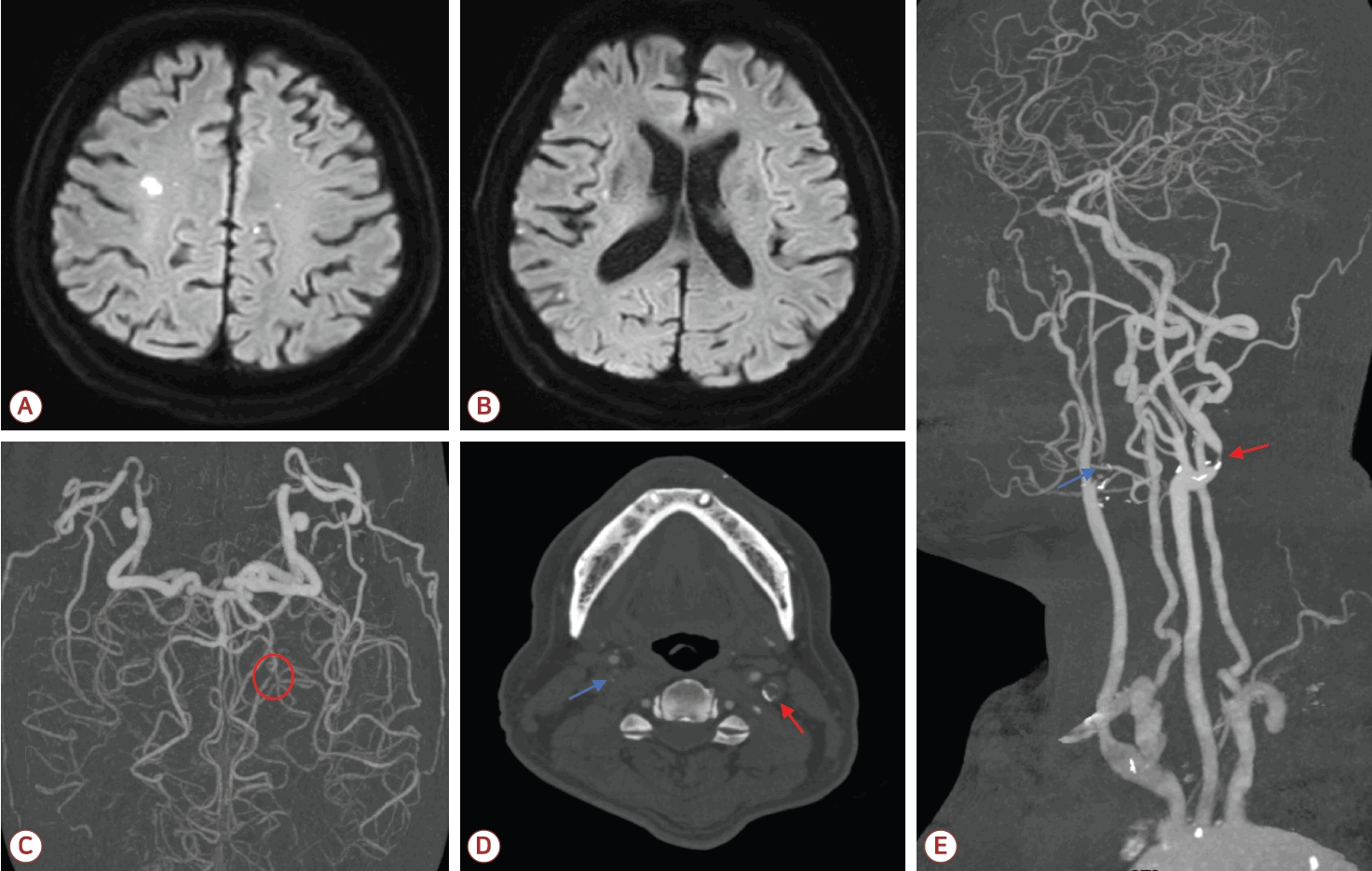
Diffusion-weighted imaging (DWI) and computed tomography angiography on admission. (A, B) Scattered areas of high signal intensity were observed on DWI in both frontal lobes and the right temporo-parietal region. (C) Focal significant stenosis was noted in the left P2 segment (red circle). (D, E) Severe stenosis was observed at the right carotid bulb (blue arrow), with diffuse narrowing of the right distal internal carotid artery. Focal severe stenosis was also present at the left carotid bulb (red arrow).
좌안 시력 저하가 있어 좌측 경동맥협착에 대해 우선 치료하기로 하였으며 입원 2일째 좌측 경동맥스텐트삽입술을 시행하였다(Fig. 2). 원래는 경동맥스텐트삽입술 후 과관류증후군(hyperperfusion syndrome)을 고려하여 수축기혈압을 140 mmHg 미만으로 보는 경우가 많으나, 우측 경동맥의 협착이 심했기 때문에 목표 수축기혈압을 100-160 mmHg 사이로 정하고 0.9% 생리식염수를 80 mL/h로 투여하며 필요시 페르디핀(perdipine)이나 노르에피네프린(norepinephrine)을 투여하기로 하였다. 환자는 시술 후 수축기혈압이 79 mmHg까지 저하되어 노르에피네프린 정맥 주사 투여를 시행하였고 이후 수축기혈압은 100-140 mmHg 정도로 유지되었다. 입원 3일째 시행한 경동맥초음파에서 스텐트 삽입 부위의 혈류는 최대 수축기속도 121 cm/s, 이완기말속도 31.3 cm/s로 양호하였고 좌안 시력은 호전되는 양상을 보였다. 혈관조영술에서 보이는 좌측 눈동맥의 혈류도 시술 전에 비해 호전된 것으로 판단되었다(Fig. 2). 하지만 경동맥초음파에서 우측 근위부 내경동맥의 최대 수축기속도는 484 cm/s, 이완기말속도는 272 cm/s로 매우 빨랐고 좌측 경동맥으로의 혈류 전환 및 혈압 저하 때문에 우측 경동맥 영역에도 뇌경색이 생길 것을 염려하여 입원 4일째 우측 경동맥스텐트삽입술을 추가로 시행하였다(Fig. 2). 당시 시점으로는 양쪽 경동맥에 모두 스텐트를 삽입한 상태였기 때문에 과관류증후군 발생 가능성이 높다고 판단하였고 목표 수축기혈압을 100-140 mmHg로 변경하여 엄격하게 조절하려 하였다. 하지만 시술 후 수축기혈압이 70 mmHg대까지 저하되었고 승압제 투여 속도를 조절하였다.
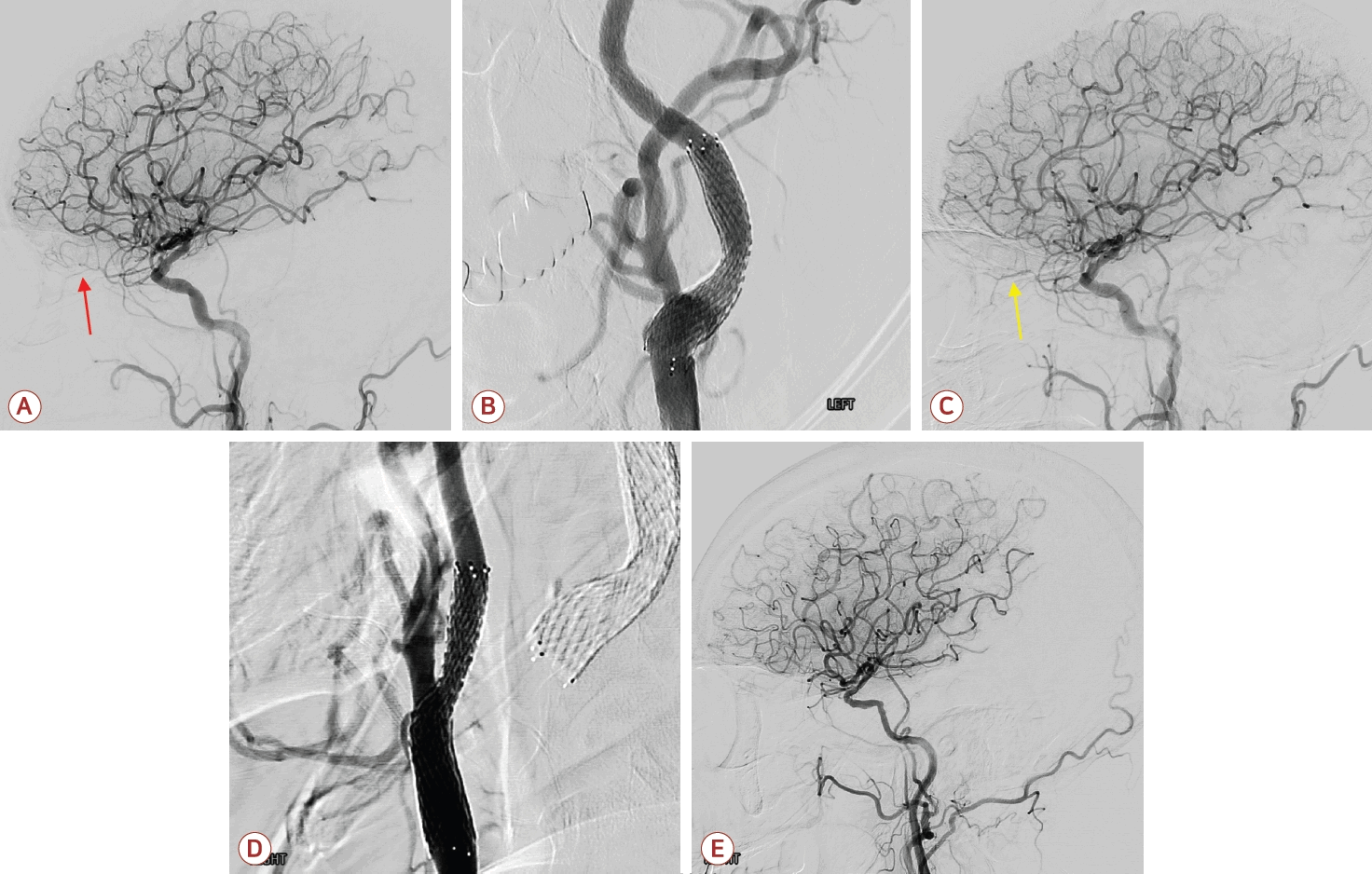
Internal carotid arteriography after carotid stenting. (A) Weak flow in the left ophthalmic artery was observed on the left internal carotid artery angiogram before left carotid artery stenting (red arrow). (B) The stent was successfully deployed in the left carotid bulb. (C) After left carotid artery stenting, improved flow in the left ophthalmic artery was observed (yellow arrow) and no immediate thromboembolic event was observed. (D) The stent was also successfully deployed in the right carotid bulb. (E) Flow through the right internal carotid artery markedly improved, and no immediate thromboembolic event was observed.
이후 환자는 과민, 불안 등의 섬망 의심 증상이 발생하였고 우측 시야 결손이 동반되었으며 NIH뇌졸중척도(National Institutes of Health Stroke Scale, NIHSS)가 8점으로 악화되었다. 섬망 증상 발생 후 시행한 뇌MRI에서 우측 후하소뇌동맥(posterior inferior cerebellar artery) 및 좌측 PCA 영역에 고신호강도 병변이 관찰되었다. CTA에서는 좌측 PCA 혈류가 이전보다 감소하였고 기존에 협착이 있던 제2분절 이후로는 혈류가 관찰되지 않았다(Fig. 3).
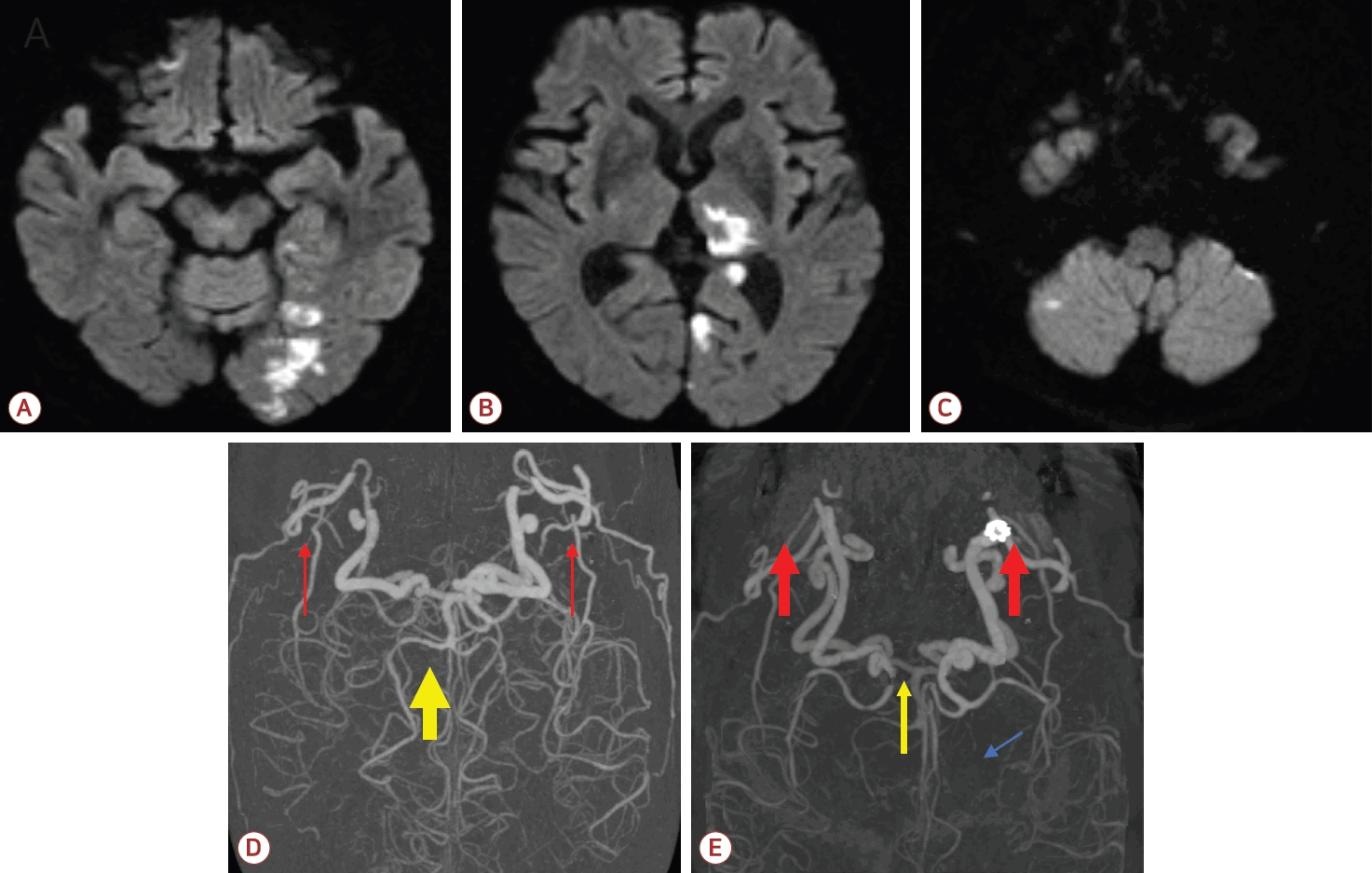
Diffusion-weighted imaging (DWI) and computed tomography (CT) angiography performed after the patient became delirious. (A, B) Areas of high signal intensity on DWI were observed in the left posterior cerebral artery (PCA) territory, including the left occipital lobe and thalamus. (C) Additional high signal intensity was noted in the right cerebellum. (D) Compared with CT angiography before stenting, (E) CT angiography after bilateral carotid stenting demonstrated diminished flow in the left PCA, with no distal flow beyond the pre-existing left P2 segment stenosis (blue arrow). This finding may be attributed to flow diversion toward both internal carotid arteries and relatively reduced posterior circulation flow after carotid artery stenting. Red arrows indicate internal carotid artery flow and yellow arrows indicate posterior circulation flow in D and E.
환자는 쿠에티아핀(quetiapine)과 발프로산(valproic acid)으로 섬망 증상을 조절하였으며 입원 15일째 섬망 증상이 호전되고 신경학적 상태가 안정되어 퇴원하였다. 퇴원 후 외래에서 항혈소판제 치료를 지속 중이다. 본 증례 보고에 대하여 고려대학교구로병원 의학연구심의위원회(Institutional Review Board, IRB)의 승인을 받았다(IRB No. 2025GR0569).
고 찰
경동맥스텐트삽입술 후 시술을 시행한 쪽의 혈류는 증가하지만 반대쪽 혈류는 일반적으로 크게 변화하지 않는다[3]. 이는 스텐트삽입술을 시행한 경동맥으로의 혈류가 증가하여 반대쪽 경동맥으로의 혈류가 감소하더라도 전교통동맥(anterior communicating artery)을 통한 곁순환(collateral circulation)이 반대쪽 전순환(anterior circulation)을 유지하기 때문으로 판단된다. 후순환과 전순환 사이에도 후교통동맥(posterior communicating artery)이라는 곁순환 통로가 존재하지만 후교통동맥이 태아형(fetal type)이 아닌 경우에는 큰 역할을 하지 못할 것으로 예상된다.
본 환자의 경우 좌안 시력 저하로 좌측 경동맥스텐트삽입술을 시행하였다. 이로 인하여 좌측 경동맥으로의 혈류는 증가하였으나 좌측 경동맥으로의 혈류 전환, 혈압 저하 등의 이유로 상대적으로 우측 경동맥, 특히 폐색 직전 상태의 경동맥으로의 혈류가 감소할 것이 예상되었다. 입원 직후 시행한 뇌MRI에서 우측 중대뇌동맥 경계 부위 뇌경색이 확인되기도 하였고 좌측 경동맥스텐트삽입술 이후 시행한 혈관조영술에서 전교통동맥을 통한 곁순환도 좋지 않았기 때문에 우측 경동맥 상태가 좋지 않은 상태에서 혈류 감소가 지속될 경우 우측 경동맥 내 혈액 정체 및 혈전 형성이 발생할 가능성이 있을 것으로 판단되어 좌측 경동맥스텐트삽입술 2일 만에 우측 경동맥스텐트삽입술도 시행하였다. 그러나 시술 후 섬망 증상이 발생하였고 시행한 뇌MRI에서 PCA 영역 위주의 후순환 뇌경색이 확인되었다. 환자의 초기 영상 검사에서는 왼쪽 PCA에 심한 협착이 있었고, 여러 영상에서 왼쪽 후교통동맥을 통한 곁순환이 충분히 발달되어 있지 않은 것으로 확인되었다. 또한 양측 경동맥 모두에 스텐트를 삽입한 후 일시적인 혈압 저하가 크게 있었음을 고려할 때 후순환 뇌경색의 발생 기전은 양측 경동맥으로의 혈류가 증가하여 상대적으로 후순환으로의 혈류가 감소하고 여기에 혈압 저하가 겹치면서 저관류성(hypoperfusion) 뇌경색이 발생하였으며, 특히 협착이 심했던 왼쪽 PCA 영역에서 뇌경색이 주로 발생한 것으로 추정된다. 일부 연구에서는 시술 중 기구가 대동맥궁(aortic arch)을 통과할 때 죽상경화판(atherosclerotic plaque)이 손상되어 다른 영역에도 뇌경색이 발생할 수 있다고 보고하지만[4] 본 환자의 경우 대동맥궁 및 양측 쇄골하동맥(subclavian artery)에는 심한 죽상경화가 관찰되지 않았다.
본 증례는 경동맥스텐트삽입술이 상당한 혈역학 변화를 수반하며, 특히 경동맥 외 다른 대뇌혈관에도 심한 협착이 있는 경우 시술 후 다른 영역에서 뇌경색이 발생할 수 있음을 보여준다. 경동맥스텐트삽입술을 시행할 때에는 시술 혈관뿐 아니라 전체 대뇌 혈류 상태의 변화를 수반할 수 있으므로 곁순환 상태를 포함하여 경동맥 외 다른 대뇌 혈관 상태를 함께 고려해야 할 것이다. 잘 알려져 있듯이 과관류증후군을 예방하기 위하여 혈압을 지나치게 높게 유지하지 않는 것이 중요하다[5]. 이전 연구에 따르면 경동맥스텐트삽입술 후 혈압은 과관류증후군을 예방하기 위하여 140/90 mmHg 이하로 조절하는 것이 권고되지만[6] 본 증례와 같이 다른 혈관에 심한 협착이 관찰되고 곁순환이 충분하지 않은 경우에는 저관류성 뇌경색 발생 위험이 있으므로 목표 혈압을 덜 엄격하게 설정하고 심한 혈압 저하도 예방하는 것이 좋겠다. 경동맥스텐트 삽입 시 혈관 벽이 기계적으로 신전될 경우 경동맥동(carotid sinus) 내 압력수용기(baroreceptor)가 자극되고 부교감신경계 활성화로 인하여 저혈압과 서맥이 발생할 수 있다[7]. 이를 예방하기 위하여 수액 공급을 통해 부족하지 않은 체액 상태를 유지해야 하며 필요시 노르에피네프린, 도파민 등의 승압제를 적극적으로 사용해야 하겠다. 양측 경동맥스텐트삽입술 시술 시 시술 간격에 대해서는 구체적인 합의는 아직 없지만 많은 연구에서 1-3개월 사이의 간격을 두고 있고, 연구에 따라 양측 경동맥스텐트를 동시에 삽입하는 것을 선호하는 경우도 있다[8,9]. 본 증례에서도 적절한 시술 간격을 정하는 것은 매우 어렵지만 한쪽 경동맥에 스텐트삽입술을 시행한 이후 발생할 수 있는 혈역학적 불안정성으로 인하여 반대쪽 경동맥을 통한 혈류에도 영향을 줄 수 있기 때문에 양쪽 경동맥의 협착 정도와 시술 이후 혈압 추이 등을 종합적으로 고려하여 시술 간격을 정할 필요가 있어 보인다.