전실어증으로만 발현된 연수막골수종증
Leptomeningeal Myelomatosis Manifesting as Isolated Aphasia
Article information
Trans Abstract
Leptomeningeal myelomatosis represents an uncommon but clinically consequential form of extramedullary disease. Because its manifestations frequently overlap with vascular and infectious conditions, timely recognition is challenging. In particular, isolated speech disturbance without accompanying motor deficits can be misattributed to acute ischemic stroke or focal seizures, potentially delaying appropriate therapy. Here, we report a case of 81-year-old female patients presenting with global aphasia. In this case, brain magnetic resonance imaging and cerebrospinal fluid study including cytology demonstrated leptomeningeal involvement by multiple myeloma.
다발골수종(multiple myeloma)은 골수 내에서 비정상적인 단클론형질세포(monoclonal plasma cell)가 과증식하여 발생하는 혈액암의 일종이다. 정상적으로 형질세포는 항체를 생성하여 감염을 방어하지만 다발골수종에서는 암세포가 비정상적인 단백질(주로 단클론면역글로빈 또는 M-단백)을 만들어 내고 골수 내 건강한 세포를 대체하며 다양한 장기 손상을 초래한다[1]. 다발골수종에서 중추신경계 침범 시 증상은 두통, 의식 변화, 뇌신경마비, 감각 저하, 위약 등 다양한 신경계 증상으로 나타날 수 있다[2,3]. 본 증례처럼 실어증과 같은 언어장애로의 갑작스러운 발현은 급성 허혈뇌졸중이나 일과성허혈발작, 초점발작 등과 혼동될 수 있어 초기 치료 방향에 중대한 영향을 미칠 수 있다. 저자들은 연수막골수종증으로 인하여 뇌실질 침범 없이 전실어증 단독으로 발현한 증례를 경험하여 보고하고자 한다.
증 례
81세 여자가 내원 당일 발생한 언어장애를 주소로 응급실에 왔다. 환자는 비파열 뇌동맥류로 결찰술을 받은 수술력이 있었고 열공경색, 다발골수종의 병력이 있었다. 환자는 2022년 7월 20일 다발골수종을 진단받았으며 다발골수종 2기에 해당하였다. 진단 후 vortezomib, melphalan, prednisone 치료를 8주기(cycle), revlimid + dexamethasone과 zomebon 4 mg 치료를 21주기, 이후 cyclophosphamide, thalidomide, dexamethasone 치료를 하였으나 효과가 없어 daratumumab을 복용 중인 상태로 전신 다발골수종이 잘 조절되고 있지 않았다. 환자는 다발골수종으로 평소 전신 위약감이 있어 지팡이로 보행은 하였으나 의사소통 능력에는 아무런 문제가 없었으며 내원 당일 아침에 혈액종양내과 정기 외래를 방문하기 위하여 준비를 할 때까지는 평소와 다름없이 의사소통이 원활하였다. 이후 차로 이동하던 중 갑작스럽게 묻는 말에 동일한 말만 반복하는 모습을 보였고 증상은 계속 지속되었다. 내원 시 혈압은 156/79 mmHg로 약간 높았고 이외의 활력징후는 정상이었다. 신경계 진찰에서 의식은 깨어있었으나 유창성, 이해 능력, 따라 말하는 능력이 모두 소실된 전실어증이 확인되었다. 팔다리 위약감 및 안면마비, 안구편위는 관찰되지 않았고 동공크기와 동공반사는 정상이었다. 이외의 국소신경학적 결손은 확인되지 않았다.
증상 발생 4시간 30분 이내 내원하였고 뇌전산화단층촬영(computed tomography, CT)에서 뇌출혈은 확인되지 않아 급성 뇌경색 가능성을 우선 고려하여 혈전용해제를 투여하였다. 이후 시행한 뇌자기공명영상(magnetic resonance imaging, MRI)에서 왼쪽 측두-두정엽피질, 뇌섬엽에 확산강조영상(diffusion weighted image, DWI)에서 고신호강도(Fig. 1-A), 대뇌 반구간 수조, 양측 실비우스 수조, 왼쪽 반구 수조에 액체감쇠역전회복영상(fluid attenuated inversion recovery, FLAIR)에서 고신호강도(Fig. 1-B), 연수막에 T1조영증강영상에서 조영증강이 확인되었다(Fig. 1-C). 뇌관류 강조 MRI에서 관류 증가나 감소 소견 없이 정상이었고 경동맥CT혈관조영술과 뇌내자기공명혈관조영(intracranial magnetic resonance angiography)에서 혈관의 협착 소견 또한 관찰되지 않았다. 또한 DWI에서 보이는 고신호강도가 뇌실질의 침범없이 피질(cortex)을 따라 형성되어 있어 급성 뇌경색의 가능성이 낮다고 판단하여 혈전용해제 투여를 중단하였다.
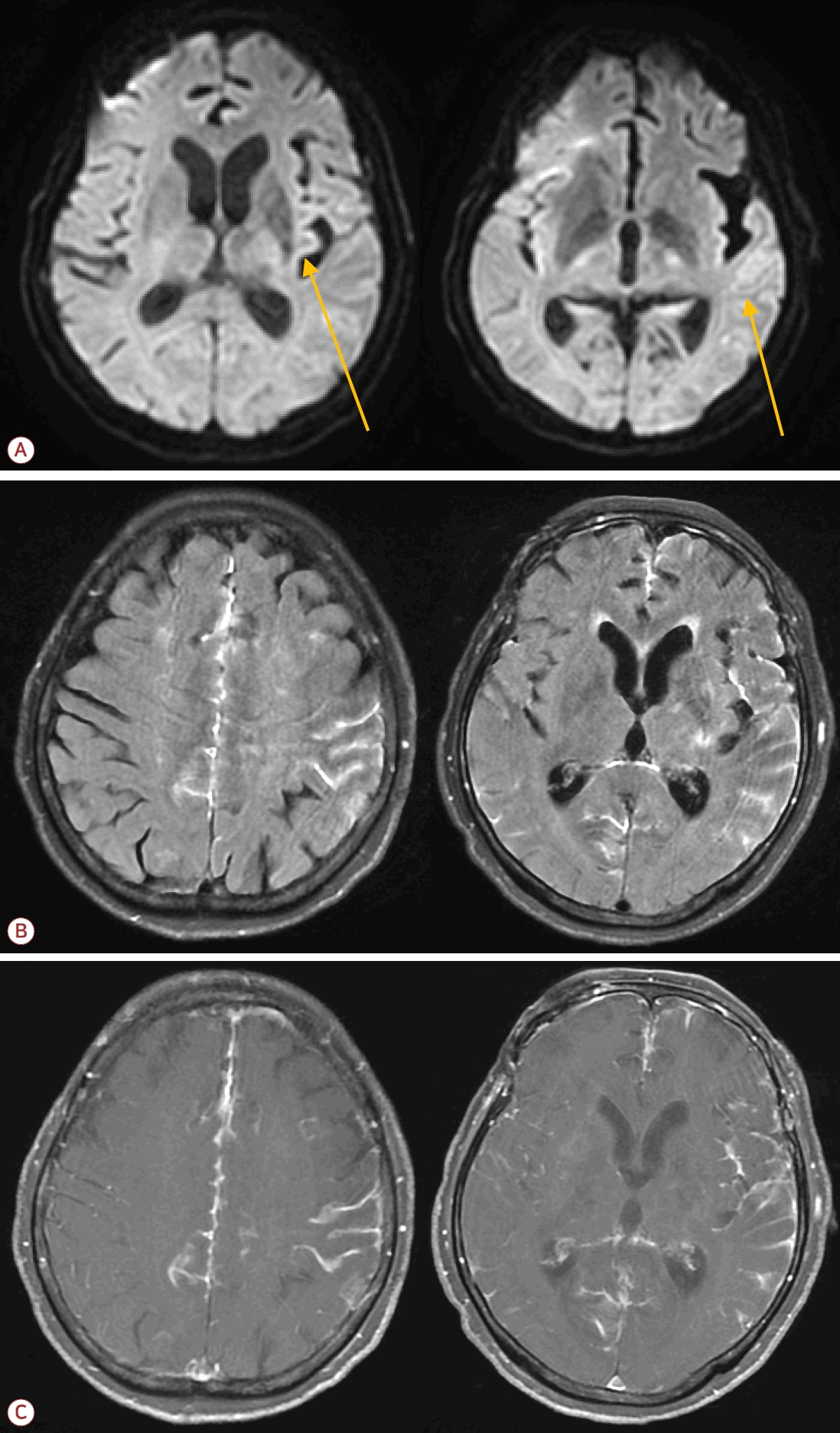
(A) Brain magnetic resonance imaging of the patient. Diffusion-weighted image shows high signal on left parieto-temporal cortex and insula (yellow arrows). (B) T2-FLAIR hyperintensity observed in the interhemispheric cistern, both Sylvian cisterns, and left hemispheric cistern. (C) T1-enhanced image shows leptomeningeal enhancement. FLAIR; fluid attenuated inversion recovery.
C-반응단백질(C-reactive protein), 적혈구침강속도(erythrocyte sedimentation rate)를 포함한 혈액검사는 모두 정상이었다. 뇌척수액 검사에서 총핵세포수(total nucleated cell, TNC) 62/mm3, 백혈구 6/mm3, 단백질 122.5 mg/dL, 포도당 47 mg/dL였다. TNC와 백혈구 수의 차이가 심하여 세포 검사(cytology)를 의뢰하였고 뇌염 가능성에 대해 아시클로버(acyclovir) 1 mg/kg과 스테로이드 펄스 요법을 시행하였다. 뇌파 검사에서 7-8 Hz의 느린 배경파 이외의 경련파는 확인되지 않았으나 발작장애 가능성을 배제하지 못하여 레베티라세탐(levetiracetam) 500 mg bid 투여하였다. 추적 신경계 진찰에서 증상 호전 없이 전실어증이 그대로 확인되었다.
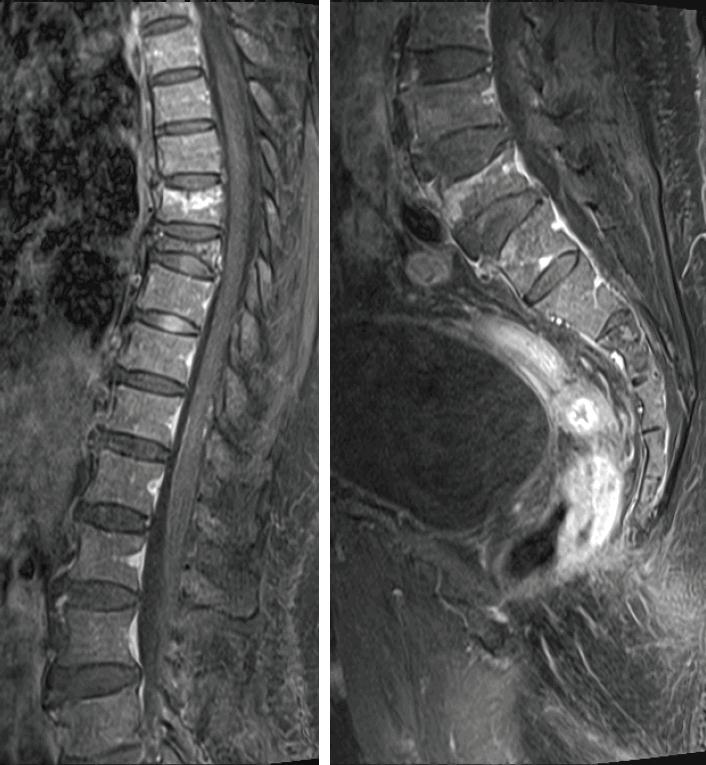
이후 뇌척수액 세포 검사에서 형질세포 95%, 림프구 2%, 대식세포-단핵구 3%로 다발골수종(multiple myeloma)의 중추신경계 침범에 합당한 소견을 보였다. 바이러스, 곰팡이, 결핵에 대한 검사는 모두 음성이었다. 다발골수종의 척수 침범을 확인하기 위하여 시행한 척수MRI에서 경추, 흉추, 요추, 천골, 양측 늑골, 양측 골반에 다발성 병변이 관찰되었으며 조영증강과 확산 제한이 동반되는 T1 골수 신호 양상이 확인되었다(Fig. 2). 추적 뇌파 검사에서 이전 뇌파와 차이가 없어 레베티라세탐을 중단하였고 연수막골수종증(leptomeningeal myelomatosis) 치료를 위하여 혈액종양내과에 의뢰하였다. 혈액종양내과 전과 후 전뇌 방사선 요법(whole brain radiation therapy)이나 수막 내 화학 요법(intrathecal chemotherapy) 없이 경구 약제 pomalide/dexamethasone 4 mg을 시작하여 5개월째 외래에서 추적 관찰 중으로 실어증이 일부 호전되는 양상을 보였다.
고 찰
다발골수종은 단클론형질세포의 증식으로 인하여 골수 내에서 다양한 장기를 침범하는 질환으로 골파괴, 고칼슘혈증, 빈혈, 신부전 등의 전신 증상을 일으킨다[2,4,5]. 다발골수종의 중추신경계 침범은 전체 다발골수종 환자의 0.3-1.0% 미만에서만 보고되고 있다. 그중에서도 연수막(leptomeninges)을 직접 침범하는 연수막골수종증은 다발골수종 환자의 0.02-0.30%에서만 발생하는 것으로 알려져 있다[2,4]. 임상 증상은 병변 부위에 따라 다양하나 주로 두통, 혼돈, 시야장애, 뇌신경마비, 감각 저하, 위약, 경부 강직 등이 나타날 수 있다[5].
국내에서 다발골수종이 중추신경계를 침범한 사례는 보고된 적이 있고[6] 해외에서 다발골수종의 중추신경계 침범이 연수막골수종증으로만 나타나거나 임상 양상으로 실어증이 나타난 사례는 보고된 적이 있다[3,7]. 전실어증은 좌측 대뇌반구의 광범위한 경색으로 인하여 주로 발생하는데, 저자들은 본 증례의 경우 DWI에서 왼쪽 측두-두정엽피질, 뇌섬엽에만 고신호강도를 보인 점으로 미루어 볼 때 이 부위의 연막 침범에 의하여 실어증 단독으로 임상 양상이 나타났을 것으로 추정하였다. DWI에서 연막 침범 부위의 고신호강도에 대해서는 두 가지 기전으로 설명된다. 악성 형질세포의 연수막 및 뇌막하공간 내 고도 침착으로 수분 확산이 제한될 수 있고[8] 침투하는 악성 세포들이 Virchow-Robin공간을 따라 주변 관통혈관(penetrating arterioles)으로 침투하여 미세경색을 야기할 수 있다[9].
또한 연수막골수종증은 비정형형질세포가 뇌척수액공간으로 따라 파종되어 연막을 침범하는 형태로 진단을 위해서는 뇌MRI와 뇌척수액 검사가 필수적이다. 뇌MRI에서 DWI나 FLAIR의 고신호를 동반하기도 한다[10]. 뇌척수액 검사에서는 단백질 증가와 세포 수 증가가 흔하고 세포 검사에서 단클론형질 세포가 검출될 경우 확진된다[9]. 본 증례처럼 TNC와 백혈구 수의 차이가 심할 경우 형질세포가 전체 핵세포의 대부분을 차지하고 있음을 시사하며 세포 조성의 확인을 위하여 세포 검사를 고려해야 한다.
결론적으로 해외에서 다발골수종의 중추신경계 침범에 의하여 실어증이 나타난 경우는 몇 차례 있으나 본 증례는 뇌실질의 침범 없이 연수막골수종증이 급성으로 실어증 단독으로만 나타난, 허혈뇌졸중 및 중추신경계 감염과의 감별이 중요한 사례로써 해부학적 고찰과 함께 이를 보고한다.