자발두개내압저하의 진단과 치료
Current Concepts in the Diagnosis and Management of Spontaneous Intracranial Hypotension
Article information
Trans Abstract
Spontaneous intracranial hypotension (SIH) is an underrecognized cause of secondary headache resulting from spinal cerebrospinal fluid (CSF) leakage. Although traditionally considered a benign and self-limiting condition, SIH is now known to be associated with substantial disability and potentially serious complications when diagnosis and treatment are delayed. The clinical presentation is heterogeneous, often leading to misdiagnosis and prolonged diagnostic latency. Recent advances have shifted the conceptual framework of SIH from a simple reduction in CSF pressure to a disorder of CSF volume depletion with distinct etiologic subtypes, including ventral dural tears, lateral dural defects associated with meningeal diverticula, and CSF-venous fistulas. Accordingly, diagnostic strategies have evolved toward a stepwise integration of clinical history with targeted imaging modalities. Contrast-enhanced brain magnetic resonance imaging (MRI) and whole-spine MRI serve as essential initial tools to establish the diagnosis and assess complications, while dynamic myelographic techniques such as digital subtraction myelography and dynamic or decubitus computed tomography myelography play a critical role in localizing the site and mechanism of CSF leakage. Management of SIH has similarly progressed toward subtype-based, individualized treatment. Epidural blood patching remains the mainstay of initial therapy, but its effectiveness varies depending on leak type and chronicity. In selected patients, surgical repair or endovascular embolization offers definitive treatment. This review summarizes current concepts in the diagnosis and management of SIH and proposes a practical diagnostic and therapeutic algorithm, while also addressing unmet needs and real-world limitations within the Korean healthcare system.
서 론
자발두개내압저하(spontaneous intracranial hypotension, SIH)는 뇌척수액(cerebrospinal fluid, CSF)의 누출에 의해 발생하는 질환으로, ‘자발’이라는 명칭에서 볼 수 있듯이 경막천자 후 두통과 같은 외상이나 의인성 요인에 의한 이차 두개내압저하와는 구별된다[1].
SIH의 연간 발생률은 인구 10만 명당 약 3-5명으로 추정되나 임상 양상이 다양하고 질환에 대한 인지도가 아직 충분하지 않아 여전히 과소 진단(underdiagnosis)과 오진(misdiagnosis)이 흔한 질환이다[2]. 이러한 특성을 고려할 때 실제 유병률은 보고된 수치보다 더 높을 가능성이 있으며, 향후 진단 기술의 발전과 인식 개선에 따라 환자 수는 더욱 증가할 것으로 예상된다.
SIH는 유아기부터 노년기까지 모든 연령층에서 발생할 수 있으나 대부분은 경제적, 사회적으로 활동이 활발한 젊은 연령층(35-55세)에서 발생한다[1]. 두통 자체의 고통뿐 아니라 급성 발병 후 장기간 누워 있어야 하는 질환의 특성으로 인하여 직업 활동과 일상생활이 갑작스럽게 중단되는 경우가 많다. 최근의 메타분석 연구에서는 급성기 SIH 환자들의 삶의 질을 EuroQol 시각상사척도(visual analogue scale)로 평가한 결과 평균 38.9점(100점 만점)으로 보고되었다[3]. 이는 유방암(약 75점)이나 폐암(약 68점) 환자들보다도 현저히 낮은 수준으로, SIH가 환자 개인에게 매우 심각한 신체적, 정신적 부담을 초래한다는 점을 알 수 있다[4,5].
SIH를 임상적으로 더욱 주목해야 하는 또 다른 이유는 과거에 비교적 양호한 예후를 보이는 양성 질환으로 인식되었던 것과 달리 다양한 중증 합병증이 동반될 수 있다는 점이다(Fig. 1). 급성기에는 경막하혈종(subdural hematoma), 뇌정맥동혈전증(cerebral venous sinus thrombosis), 뇌하강(brain sagging)에 따른 뇌간 압박 및 뇌탈출로 사망에 이르는 경우도 있다[6-8]. 또한 만성적인 경과를 취하는 환자에서는 표재철침착증(superficial siderosis), 양측 상완근 위약을 특징으로 하는 양팔 근위축증(bibrachial amyotrophy), 인지기능 저하를 동반한 뇌하강 치매(brain sagging dementia)와 같은 합병증이 발생할 수 있다[9-11].
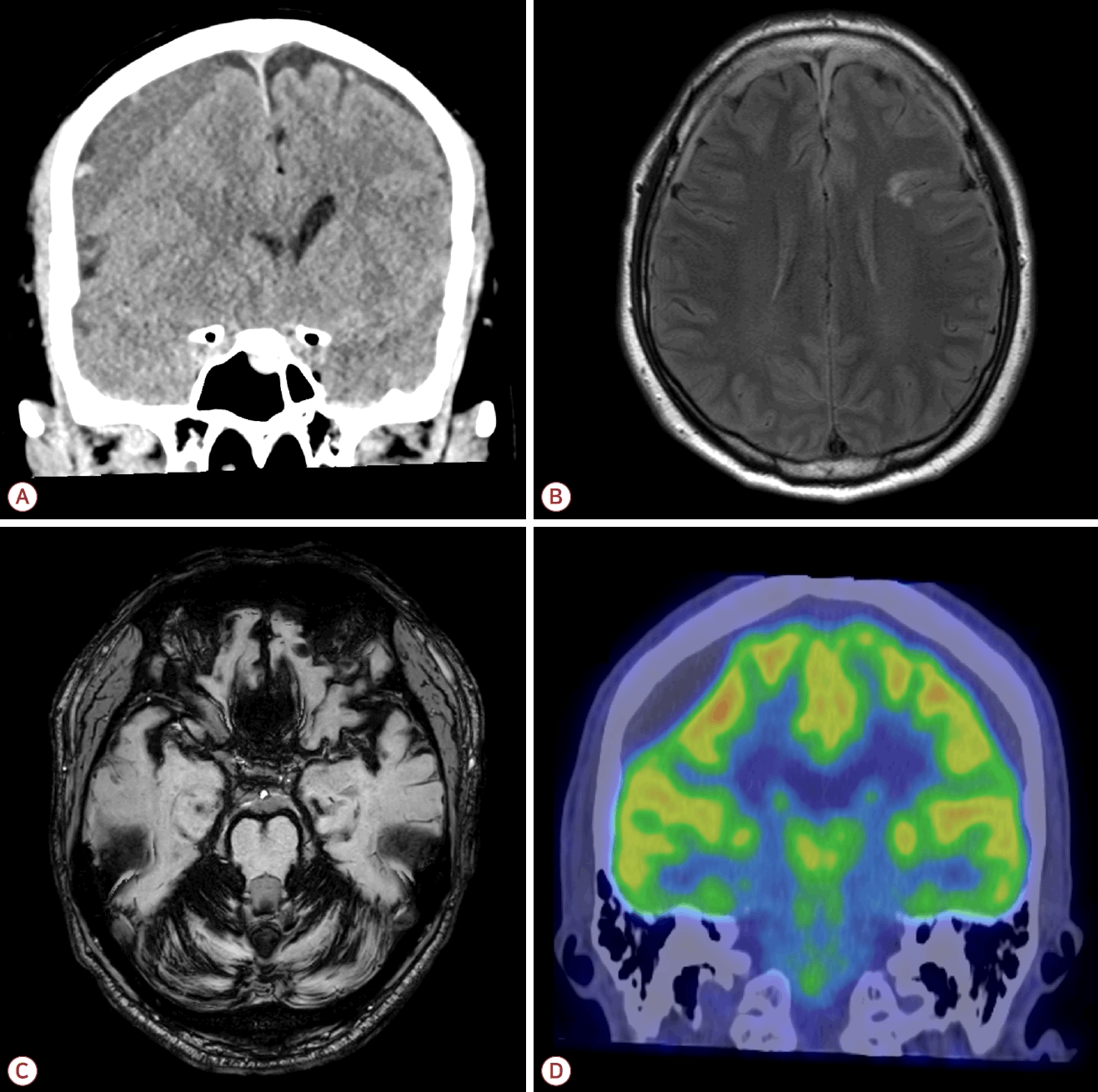
Complications of spontaneous intracranial hypotension. (A) Subdural hematoma. (B) Cerebral venous sinus thrombosis. (C) Infratentorial superficial siderosis. (D) Brain sagging dementia.
최근 10여 년간 SIH의 진단과 치료에는 중요한 패러다임의 변화가 나타나고 있다. 척추 뇌척수액 누출의 다양한 병태생리적 아형(subtype)이 규명되면서 이를 진단하기 위한 영상 기법과 치료 전략 또한 빠르게 발전하였다[12]. 그러나 이러한 변화에도 불구하고 용어와 분류 체계의 통일성이 부족하고 대륙 및 국가별로 진단 및 치료 접근법에 상당한 차이가 존재하는 것이 현실이다[13,14].
이에 본 종설에서는 최근의 연구 결과를 바탕으로 SIH의 진단과 치료에 대한 최신 개념을 정리하고 임상 진료에서의 실제적인 접근 전략을 제시하고자 한다.
본 문
1. 병태생리와 분류
1) SIH의 병태생리
SIH의 병태생리는 단순한 뇌척수액 압력 저하보다는 뇌척수액 용적 감소(CSF hypovolemia)라는 개념으로 이해하는 것이 적절하다[15]. 실제로 많은 SIH 환자에서 뇌척수액 개방압(CSF opening pressure)은 정상 범위이거나 경미하게 감소되어 있는 경우가 흔히 관찰되며, 이는 SIH가 반드시 측정 가능한 저압 상태를 동반하지는 않음을 시사한다. 이러한 이유로 질병 명칭에서 저압(hypotension)이라는 표현을 수정해야 한다는 주장도 제기되어 왔으나 관용적인 이유로 현재까지 명칭은 유지되고 있다.
뇌척수액 용적의 감소는 뇌를 지지하는 부력의 저하로 이어지며, 그 결과 뇌는 중력 방향으로 하강하게 된다[1]. 이러한 뇌하강(brain sagging)은 기립두통의 주요 기전으로 여겨지며 이외에도 귀 먹먹함, 이명, 어지럼증과 같은 다양한 동반 증상을 유발할 수 있다. 한편 두개강 내에서는 몬로-켈리 원리(Monro-Kellie doctrine)에 따라 뇌척수액 감소를 보상하기 위한 정맥 혈액량이 증가하고, 이는 경막 혈관의 확장과 투과성 증가를 초래하여 SIH에서 특징적으로 관찰되는 뇌영상 소견의 기초가 된다.
중요한 점은 SIH로 인한 병태생리적 변화가 단일 단계(monophasic)로 진행되지 않는다는 것이다. 뇌척수액 용적 감소에 대한 보상 기전으로 뇌척수액 생성이 증가하거나16 누출 부위 주변에 신생막(neo-membrane)이 형성되는 현상이 발생할 수 있다[17]. 이러한 변화는 SIH 환자에서 자연적으로 증상이 호전(또는 악화)되는 임상 경과를 설명하며, 때때로 뇌척수액 누출이 지속되고 있음에도 뇌영상 소견이 정상화되는 이유가 되기도 한다[18]. 결과적으로 이러한 역동적인 변화는 SIH의 진단을 더욱 까다롭게 만드는 요인으로 작용한다.
2) SIH의 기전적 분류
최근 SIH에 대한 이해는 단일한 질환 개념에서 벗어나 뇌척수액 누출의 형태와 위치에 따른 병인적 아형을 중심으로 재정립되고 있다. 이러한 분류는 단순한 병리학적 구분을 넘어 진단을 위한 영상 기법의 선택과 치료 전략을 결정하는 데 중요한 기준이 된다(Table 1).
1형 누출은 주로 전방 경막 결손(ventral dural tear)에 의해 발생한다. 이 결손은 대개 골극(microspur)에 의해 경막이 찢어지며 발생하며 흉추 상부(high thoracic level)에서 가장 흔히 관찰된다[19]. 이 유형에서는 누출된 뇌척수액이 척추강 내 경막외 공간에 고여 있게 되므로 척수영상 검사에서 뇌척수액 저류(척추종축경막외액체저류[spinal longitudinal epidural collection, SLEC])가 거의 항상 관찰되는 것이 특징이다.
2형 누출은 측방 경막 결손(lateral dural tear)에 의한 누출로 대부분 거미막 게실(arachnoid diverticulum)과 연관되어 나타난다[20]. 1형과 마찬가지로 상당수의 환자에서 뇌척수액 저류가 관찰되지만 그것이 주로 측방(lateral) 또는 후방(dorsal)에 분포하는 경우 이 아형을 의심할 수 있다[21]. 흉추 하부(low thoracic level)에서 가장 흔하게 관찰된다.
3형 누출은 뇌척수액-정맥 누공(CSF-venous fistula)을 의미하며 뇌척수액이 경막외 공간을 거치지 않고 정맥계로 직접 유입되는 형태의 누출이다. 2014년 처음 보고되었을 당시에는 매우 드문 아형으로 인식되었으나[22] 최근 영상 기법의 발전으로 진단되는 환자 수가 빠르게 증가하고 있다. 이 아형에서는 척추강 내에 뇌척수액 저류가 관찰되지 않는 경우가 많아 전통적인 척추영상 검사만으로는 진단이 어렵다. 평균 발병 연령은 1형, 2형보다 높은 50-60세이며 흉추 하부(low thoracic level)에서 가장 흔하게 관찰되지만 경추나 요추에서도 발생 가능하다[23,24].
이러한 1형, 2형, 3형 아형은 해부학적 분류에 기반한 Schievink 분류법[25]과 영상학적 소견에 기반한 Farb 분류법19에서 공통적으로 다루고 있으나 세부 아형의 정의와 표현에는 차이가 있어 문헌을 해석할 때 주의가 필요하다. 또한 최근에는 뇌척수액이 림프계로 누출되는 새로운 병태가 보고되는 등, 향후 SIH의 분류 체계는 더욱 발전할 가능성이 있다[26].
2. 자발두개내압저하의 진단적 접근
1) 병력 청취
SIH의 가장 중요한 임상적 특징은 기립두통(orthostatic headache)이다. SIH 환자의 약 98.5%에서 두통이 동반되며 이 중 약 94.5%가 기립성 양상의 두통을 호소한다[1]. 전형적인 기립두통은 머리 양측에 전반적으로 욱신거리는 양상을 띠며 기립 시 악화되고 누우면 호전되는 특징을 보인다.
이러한 기립두통은 체위 변화와 연관된 다른 질환들, 예를 들어 체위기립빈맥증후군(postural orthostatic tachycardia syndrome, POTS)이나 편두통, 특발두개내압상승(idiopathic intracranial hypertension)의 치료 과정에서도 관찰될 수 있어 감별이 필요하다. SIH의 기립두통은 대개 급성으로 발생하는 경우가 많아 환자들이 증상 시작 시점을 비교적 명확히 기억하는 반면, POTS나 편두통에서는 그런 회상이 어려울 수 있다. 특히 편두통의 경우 가만히 누워 있을 때 두통이 다소 완화될 수 있어 기립두통과 감별이 어려울 수 있다. 이때는 과거에 유사한 편두통 발작이 있었는지, 누운 자세에서 두통이 거의 완전히 소실되는지, 2-3일 이상 경과 후에도 명확한 호전 없이 일방향적인 질병 경과를 갖는지 등을 면밀히 확인할 필요가 있다.
또한 발살바수기에 의해 악화되는 기침두통(cough headache)이 기립두통으로 오인되는 경우도 있다. 기립을 위하여 자세를 변경하는 과정에서 일시적인 발살바수기가 동반될 수 있기 때문에 기립 순간 짧게 머리가 울리는 양상의 통증이라면 기립두통보다는 기침두통을 우선 고려해야 한다. 이 경우 누운 자세에서 기침을 시켜 두통 유발 여부를 확인함으로써 쉽게 감별할 수 있다. 다만 SIH의 급성기에서 경막하혈종(subdural hematoma)이 동반된 경우나 3형 누출(뇌척수액-정맥 누공)에서는 초기부터 전형적인 기립두통 대신 기침두통 양상으로 나타날 수 있어 상세한 병력 청취와 감별 진단이 매우 중요하다.
두통 외에도 SIH는 다양한 동반 증상을 유발할 수 있다. 어지럼증, 메스꺼움, 귀 먹먹함, 이명 등이 절반 이상의 환자들로부터 보고되며 뒷목 통증이나 어깨 통증이 동반되는 경우도 적지 않다[27]. 이러한 증상들은 대개 뇌하강과 연관되어 발생하지만 일부 증상은 척추강 내 뇌척수액 저류에 의해 발생하기도 한다.
비록 기립두통이 SIH의 중요한 임상적 특징이지만 질환이 만성화됨에 따라 앞서 기술한 병태생리적 변화로 인하여 이러한 기립성 양상이 점차 모호해지거나 사라질 수 있다. 실제로 일부 환자는 수개월이 지나면 기립성이 뚜렷하지 않은 만성적인 일차 두통과 유사한 양상을 보이기도 하며, 두통 자체는 호전되더라도 귀 먹먹함과 같은 비교적 경미한 증상만 지속되는 경우도 있다. 따라서 이러한 비기립성 두통으로의 변화를 인식하는 것이 중요하며 두통의 초기 발생 시점과 이후 임상 양상의 변화를 포함한 병력 청취가 진단에 중요한 단서를 제공할 수 있다.
아울러 SIH의 단기 및 장기 합병증에 대한 병력 확인도 중요하다. SIH로 인한 경막하혈종이나 뇌정맥동혈전증의 경우 발작(seizure)이나 국소 신경학적 결손을 첫 주소로 내원할 수 있다. 또한 보행장애를 주소로 내원한 환자의 뇌자기공명영상(magnetic resonance imaging, MRI)에서 원인 불명의 표재철침착증이 관찰되는 경우 SIH의 장기 합병증일 가능성을 염두에 두고 수년에서 수십 년 전 기립두통의 병력이 있었는지를 확인하는 것이 필요하다.
2) 요추천자를 통한 뇌척수액 개방압(cerebrospinal fluid opening pressure) 측정
과거에는 요추천자를 통한 뇌척수액 개방압 측정이 SIH 진단에 필수적인 검사로 여겨졌으나, 이후 다수의 연구를 통해 SIH 환자 중 상당수가 정상 범위의 뇌척수액 압력을 보인다는 사실이 밝혀지면서 현재는 일상적인 검사로 권고되지 않는다[28]. 또한 요추천자로 인하여 기존의 SIH 증상을 악화시킬 가능성도 있다. 다만 동적 척수조영술(dynamic myelography)과 같은 검사를 위하여 요추천자가 반드시 수반되는 경우나 영상 검사가 제한적인 환경에서는 뇌척수액 개방압을 보조적인 진단 수단으로 활용할 수 있다.
3) 방사성동위원소뇌수조조영(radioisotope cisternography)
과거에는 SIH 진단에 널리 사용되었던 검사이지만 현재는 더 이상 권고되지 않는다[28]. 그 이유로는 첫째, 자기공명척수조영술(magnetic resonance [MR] myelography)이나 전산화단층촬영척수조영술(computed tomography [CT] myelography)에 비해 진단 민감도가 현저히 낮다. 둘째, 침습적인 검사로 환자에게 불편을 초래하며 검사에 소요되는 시간이 길다. 셋째, 방사선 노출의 문제가 있다. 더 나아가 현재의 SIH 병인적 분류 체계에 비추어 볼 때 과거 방사성동위원소뇌수조조영의 전후면 영상에서 측방으로 누출되는 것으로 해석되었던 소견들 중 상당수는 실제 누출이 아니라 단순한 게실이었을 가능성이 있다[29].
4) 조영증강 뇌MRI
조영증강 뇌MRI는 SIH 진단에서 가장 중요한 초기 검사 방법이다. 이 검사는 SIH로 인한 전형적인 영상학적 소견을 확인하는 데 필수적일 뿐 아니라 경막하혈종과 같은 합병증의 동반 여부를 평가하는 데에도 중요한 역할을 한다. 조영증강 뇌MRI의 SIH 진단 민감도는 약 73%로 보고되고 있다[27].
SIH에서 관찰되는 대표적인 영상 소견으로는 정맥동 충혈(venous engorgement), 뇌하수체 충혈(pituitary engorgement), 광범위 경막조영증강(diffuse pachymeningeal enhancement), 뇌하강(brain sagging), 경막하삼출(subdural effusion) 등이 있다(Fig. 2). 이러한 소견들을 종합하여 SIH의 가능성을 정량적으로 평가하기 위한 지표로 베른 점수(Bern score)가 제안되기도 하였다(Table 2) [30]. 베른 점수에서 5점 이상을 고위험군으로 정의할 경우, 원 저자들의 코호트에서는 78.6%의 민감도와 98.3%의 특이도를 보였다. 그러나 한국인을 대상으로 한 연구에서는 민감도가 22.2%로 낮았던 반면 특이도는 100%로 유지되어 인구 집단 또는 아형, 증상 발현 시기에 따라 베른 점수의 진단 성능이 달라질 수 있음을 시사한다[18].
Typical brain MRI findings. (A) Brain sagging with pituitary engorgement. (B) Diffuse pachymeningeal enhancement (white arrowheads) and venous engorgement (white arrows). (C) Subdural effusion. MRI; magnetic resonance imaging.
일반적으로 정맥동 충혈과 뇌하수체 충혈이 발병 후 비교적 초기, 특히 발병 후 첫 1주 이내에 먼저 나타나고 광범위 경막조영증강과 뇌하강이 이어서 발견된다[31]. 경막 삼출은 발병 후 2-4주가 경과한 뒤에 나타날 수 있으며 삼출이나 뇌하강이 과도한 경우 교량정맥(bridging vein)의 파열로 인하여 경막하혈종으로 진행할 수 있다.
한편 임상적으로 SIH가 의심됨에도 불구하고 뇌MRI가 정상으로 보이는 경우가 약 19%의 환자에서 보고된다[27]. 이러한 소견은 개인별 뇌척수액 누출에 대한 보상 기전의 차이와 연관된 것으로 추정된다. 또한 앞서 언급한 이유로 SIH에서는 시간 경과에 따라 뇌MRI 소견이 변화할 수 있으므로 단일 시점의 영상만으로 진단을 배제하거나 확정하는 데에는 주의가 필요하다.
SIH에서는 소뇌 편도의 하강이 관찰될 수 있어 때때로 1형 히아리기형(Chiari malformation type I)과의 감별이 필요하다. 이 경우 경막조영증강, 뇌하수체 충혈, 정맥동 충혈과 같은 동반 소견의 유무를 확인하는 것이 도움이 될 수 있으며 중뇌하강을 반영하는 교뇌중뇌각(pontomesencephalic angle)의 감소 역시 감별에 유용한 지표로 제시되고 있다[32].
5) 척추MRI (spine MRI)
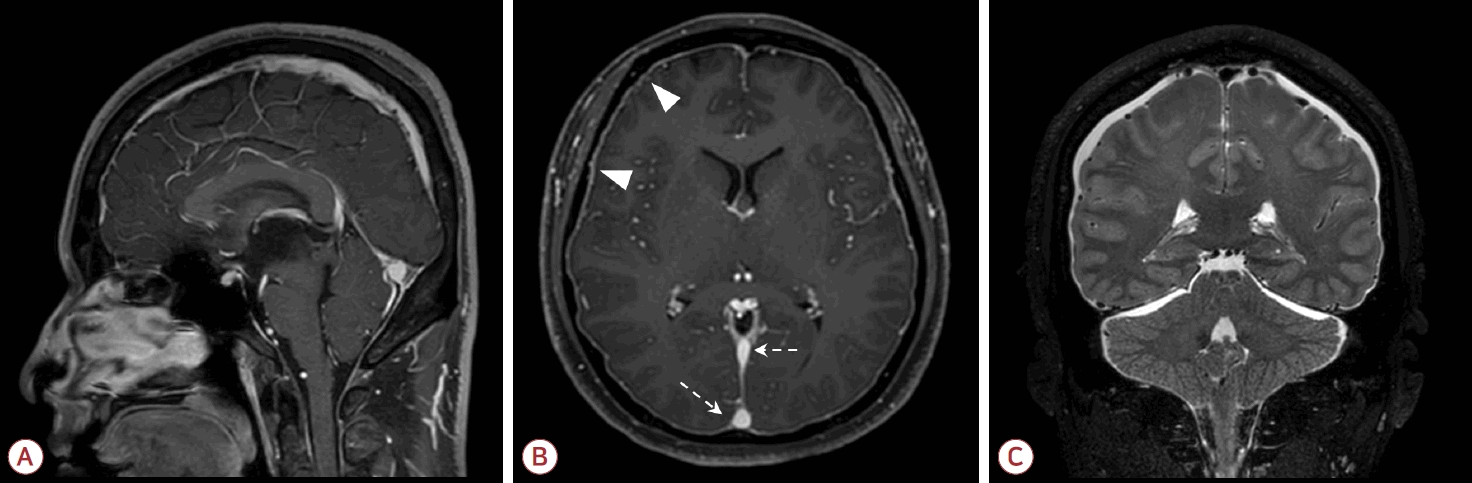
척추MRI는 조영증강 뇌MRI와 함께 SIH의 초기 진단 단계에서 필수적인 검사이다. 척추MRI에서 뇌척수액 저류가 관찰되는 경우 그 자체로 SIH의 확진에 강력한 근거가 되며, 병인적으로는 1형 또는 2형 누출을 시사한다(Fig. 3-A). 문헌에 따른 차이는 있으나 SIH 환자의 48-76%에서 척추MRI상 뇌척수액 저류가 관찰되는데[27], 척추MRI의 진단 성능은 사용되는 장비와 촬영 프로토콜에 따라 차이를 보일 수 있다. 또한 3형 누출(뇌척수액-정맥 누공)의 경우에는 기전적으로 척추MRI에서 뇌척수액 저류가 전혀 관찰되지 않는다[22]. 따라서 SIH의 진단은 척추MRI 소견만으로 이루어질 수 없으며 병력과 뇌MRI 소견을 포함한 임상 정보를 종합하여 판단해야 한다.
Spinal longitudinal epidural collection (SLEC) in spinal imaging. (A) Sagittal image of T2-weighted spinal MRI. Ventral SLEC (white arrow) is noted. (B) Axial image of heavily-T2 weighted, MR myelography. Ventral and dorsal SLEC (white arrowheads) are noted. (C) Axial image of conventional CT myelography, which was acquired in the same patient as (B). MRI; magnetic resonance imaging, MR; magnetic resonance, CT; computed tomography.
SIH 진단을 위한 척추MRI에는 여러 기법이 사용된다. 그중 자기공명척수조영술(MR myelography)은 중 T2 강조(heavily T2-weighted) 영상을 3차원적으로 재구성하는 기법으로 비침습적으로 뇌척수액 저류를 감지하는 데 탁월한 성능을 보인다(Fig. 3-B) [33]. 일부 해외 기관에서는 요추천자 후 자기공명영상용 조영제인 가돌리늄을 척수강 내에 주입한 뒤 척수조영술(intrathecal gadolinium-enhanced MR myelography)을 시행하기도 하나 가돌리늄의 척수강 내 주입은 미국 식품의약국(United States Food and Drug Administration, FDA) 및 국내에서 승인되지 않은 상태이다[34].
6) 디지털감산척수조영술(digital subtraction myelography)
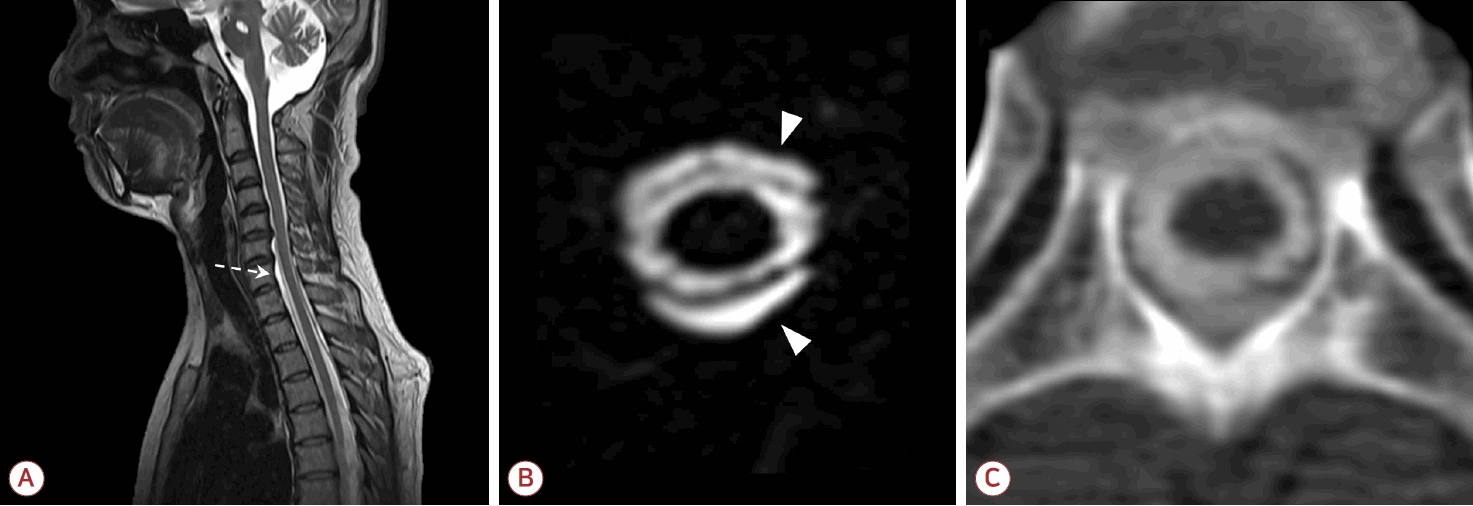
앞서 언급한 뇌MRI와 척추MRI는 SIH의 존재 여부를 진단하는 데에는 유용하지만 뇌척수액이 어디에서, 어떤 형태로 누출되고 있는지에 대한 정보는 제공하지 않는다. 이러한 한계를 보완하기 위하여 동적 척수조영술(dynamic myelography)라는 개념이 도입되었는데, 이는 요추천자 후 조영제를 척수강 내로 주입하면서 실시간으로 누출 부위를 확인하는 검사를 의미한다(Fig. 4) [14]. 최근 SIH 치료 전략에서 병인적 아형과 누출 부위에 따른 표적 치료의 중요성이 강조되면서 동적 척수조영술의 역할 역시 더욱 커지고 있다.
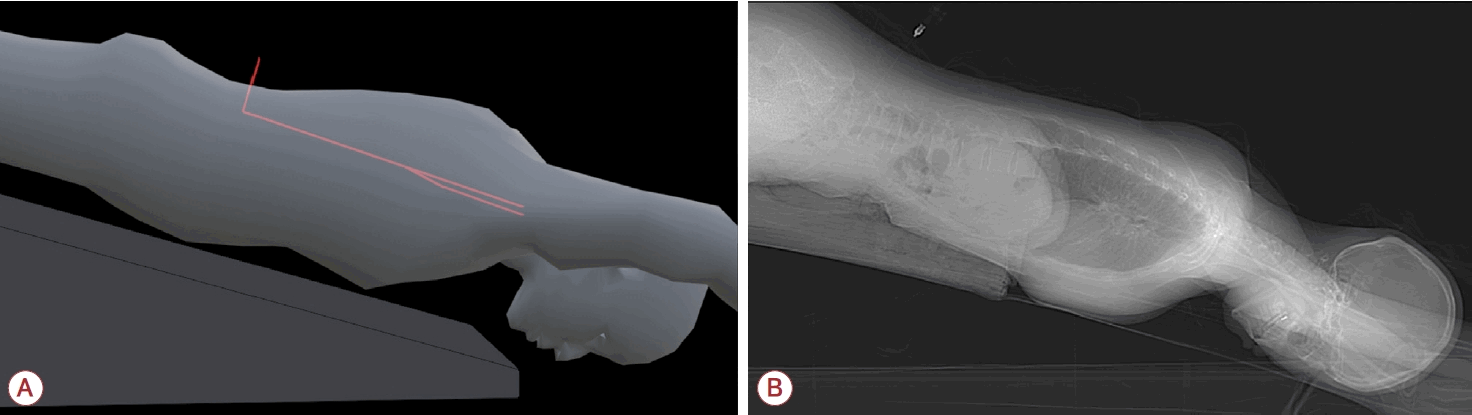
Schematic illustration of the patient’s position in dynamic myelography to detect a type 1 ventral leak. (A) 3D image showing contrast medium (red line) injected via a spinal needle flowing along the incline to identify the leak site. (B) X-ray image of a patient undergoing dynamic CT myelography. CT; computed tomography.
디지털감산척수조영술(digital subtraction myelography, DSM)은 동적 척수조영술의 한 형태로 혈관조영 장비를 갖춘 중재시술실에서 시행된다. 일반적으로 요추천자를 시행한 후 wedge foam이나 tilting table을 이용하여 조영제가 이동할 방향을 조절한다[35]. 대부분의 경우 머리를 중력 방향으로 더 낮게 위치시킨다. 검사 시 의심되는 SIH의 유형에 따라 환자의 자세를 조절하는데, 1형 누출에서는 엎드린 자세(prone position), 2형과 3형 누출에서는 옆으로 눕는 자세(decubitus position)가 주로 사용된다(Fig. 5).
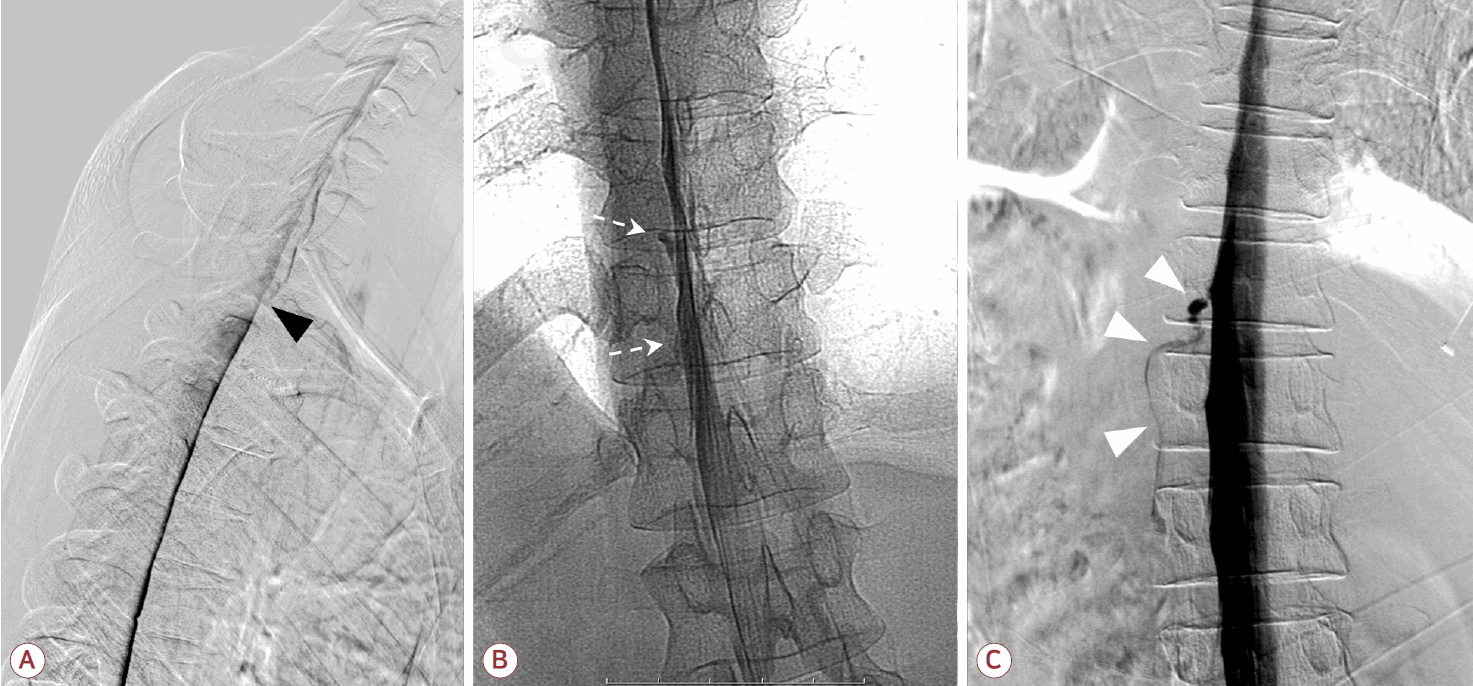
Digital subtraction myelography findings according to leak type. (A) T1-2 ventral leak (black arrowhead) in patient with type 1 leak. (B) Shoulder-type lateral leak from left T10-11 diverticula (white arrows) in patient with type 2 leak. (C) CSF-venous fistula arising from left T12-L1 nerve root sheath (white arrowheads), which is draining to external vertebral venous plexus, in patient with type 3 leak. CSF; cerebrospinal fluid.
DSM은 0.5-1.0초 간격으로 영상을 얻을 수 있어 시간 해상도가 매우 뛰어나다는 장점이 있다[14]. 그러나 X-ray를 2차원 평면 영상으로 획득하기 때문에 해부학적 구조물이나 척수강 내 조영제가 누출 부위를 가리는 경우가 발생할 수 있다. 최근엔 이러한 한계를 보완하기 위하여 조영 장비를 이용한 콘빔 CT(cone-beam CT)를 병행하기도 한다[36].
7) CT척수조영술(CT myelography)
전통적으로 CT척수조영술은 요추천자 후 조영제를 주입한 뒤 15-60분이 경과한 시점에 눕거나 엎드린 자세로 촬영하는 기법을 의미하며, 최근에는 이를 후술할 새로운 검사들과 구분하기 위하여 고식적 CT척수조영술(conventional CT myelography)로 지칭한다. 고식적 CT척수조영술은 MR척수조영술과 유사하게 척추강 내 뇌척수액 저류를 확인하는 데 사용되지만 침습적이며 MR척수조영술에 비해 진단 성능이 떨어진다는 단점 때문에 요즘은 널리 쓰이지 않는다(Fig. 3-C) [33].
그럼에도 불구하고 CT척수조영술이 다시 주목받는 이유는 이를 동적 CT척수조영술(dynamic CT myelography)로 활용하거나 3형 누출(뇌척수액-정맥 누공)을 진단하기 위한 측위 CT척수조영술(decubitus CT myelography)로 적용할 수 있기 때문이다.
동적 CT척수조영술(dynamic CT myelography)은 종종 초고속 CT척수조영술(ultrafast CT myelography)로도 불리며, 조영제가 이동하는 동안 연속적인 CT 영상을 획득하는 기법이다(Fig. 6-A, B) [37]. DSM과 유사하게 요추천자가 시행된 상태에서 CT실에서 환자를 검사 자세로 눕힌 뒤 조영제를 주입하며 촬영한다. CT의 특성상 단면 영상을 통해 매우 높은 공간 해상도를 제공한다는 장점이 있으나 DSM에 비해 시간 해상도가 떨어지고 방사선 노출량이 많다는 단점도 있다[14,38].
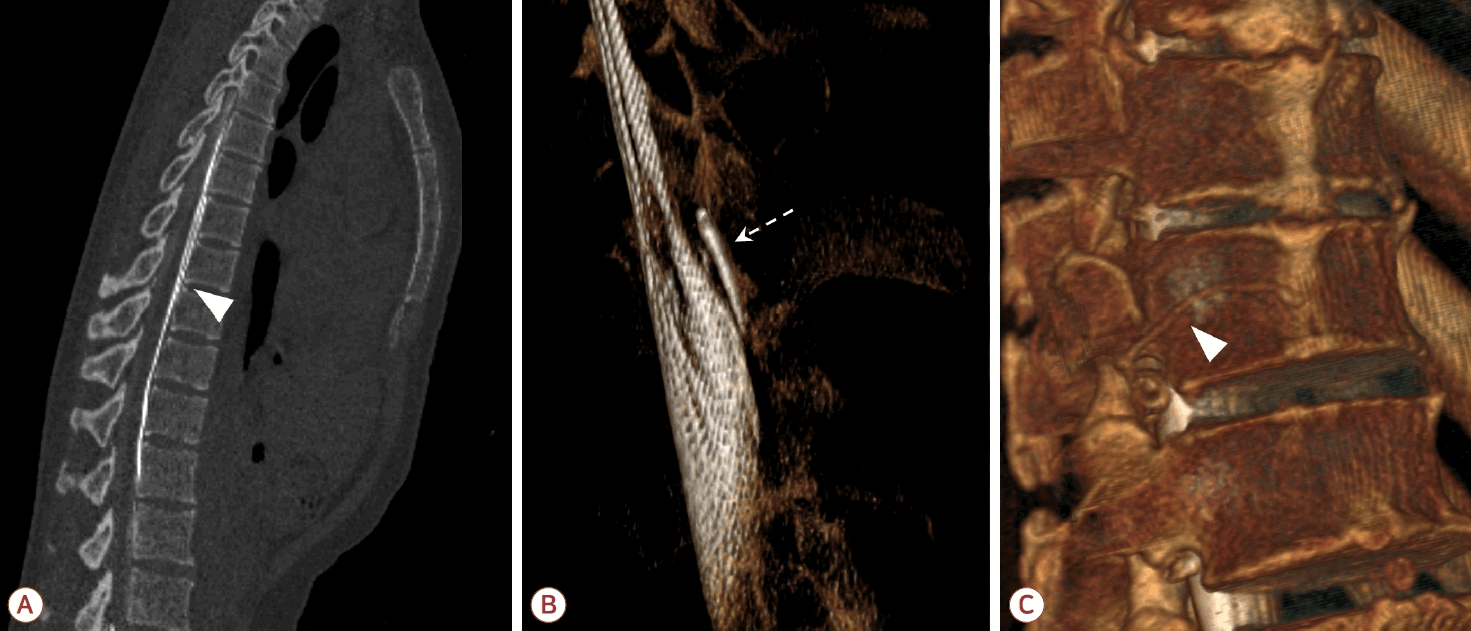
Dynamic or decubitus CT myelography findings according to leak type. (A) Sagittal view of T8-9 ventral leak in patient with type 1 leak (white arrowhead). (B) Volume-rendered image of lateral leak from left T10-11 (white arrow) in patient with type 2 leak. (C) Volume-rendered image of a CSF-venous fistula arising from right T12-L1 in patient with type 3 leak (white arrowhead). CT; computed tomography, CSF; cerebrospinal fluid.
측위 CT척수조영술(decubitus CT myelography)은 척추 MRI에서 뇌척수액 저류가 관찰되지 않는 3형 누출의 누출 부위를 진단하기 위하여 사용되는 기법이다(Fig. 6-C). 반복 촬영을 통해 시간 해상도를 높이기보다는 옆으로 누운 자세를 이용하여 조영제가 신경근초(nerve root sleeve)에 충분히 충만되도록 한 뒤 촬영하는 것이 특징이다[39]. 뇌척수액-정맥 누공은 매우 미세한 구조일 수 있으므로 0.6 mm 이하의 얇은 절편 두께로 재구성하여 판독하는 것이 권고된다.
3. 자발두개내압저하의 치료적 접근
1) 보존적 치료(conservative management)
보존적 치료 중 가장 기본이 되는 것은 절대적 침상 안정(absolute bed rest)이다[28]. 침상 안정은 SIH 환자에서 두 가지 측면에서 강력히 권장된다. 첫째, SIH의 기저 병태생리가 뇌척수액 용적 감소에 따른 뇌하강임을 고려할 때 침상 안정은 그 자체로 뇌의 부력 저하를 완화하여 두통을 포함한 다양한 동반 증상을 경감시킨다. 또한 뇌하강으로 인한 기계적 장력을 줄임으로써 경막하혈종과 같은 합병증의 발생 위험을 낮출 수도 있다[40].
둘째, 침상 안정은 뇌척수액 누출 부위에서의 누출량을 감소시켜 경막 결손 부위의 자가 치유(self-healing)를 촉진한다. 경막 결손의 자가 치유는 누출 부위에 미세한 혈전이 형성되고, 이후 염증 반응과 섬유화 과정을 거쳐 결손이 봉합되는 기전으로 이해되고 있다. 발병 후에도 기립이 지속될 경우 중력으로 인한 척수강 내 정수압이 증가하며 누출 부위에 가해지는 압력이 커져 지속적인 뇌척수액 누출이 치유 과정을 방해하는 요소로 작용할 수 있다.
충분한 수분 섭취(hydration) 역시 보존적 치료의 중요한 요소로, 뇌척수액 용적 감소를 보완하여 증상 완화에 기여할 수 있다. 유사한 맥락에서 염분 섭취를 권장하기도 한다. 복대 착용은 복압을 증가시켜 중심정맥압을 상승시킴으로써 뇌척수액 누출을 줄이는 데 도움이 될 수 있다[41].
이 외에도 근거는 제한적이나 카페인 섭취가 보존적 치료의 보조 수단으로 사용되기도 한다. 카페인은 1940년대부터 경막천자후두통(post-dural puncture headache, PDPH)의 치료에 활용되어 왔으며 코크란 리뷰에서는 PDPH 환자에서 하루 1회 경구 카페인 300 mg 투여를 권고하고 있다[42]. 참고로 일반적인 아메리카노 한 잔에 포함된 카페인 함량은 약 100-150 mg이다. 카페인은 급성기에 두통을 완화하고 뇌척수액 생성을 촉진하는 효과가 있는 것으로 알려져 있어 유사한 병태생리를 공유하는 SIH에 적용하는 것은 이론적으로 합리적이다. 이외에도 methylxanthine 계열 약물인 theophylline이나 스테로이드가 사용된 보고들이 있으나 이러한 약물 치료는 여전히 SIH에서의 근거 수준이 매우 제한적이기에 다른 치료 옵션이 부족한 상황에서 제한적으로 고려할 수 있다[41].
발병 초기에는 약 4-6주간 과도한 신체 활동을 제한하는 것이 권고되며 특히 복압을 증가시키는 행동(무거운 물건 들기, 기침, 배변 시 과도한 힘주기 등)은 뇌척수액 누출을 더 유발하거나 재발 위험을 증가시킬 수 있어 일정 기간 주의가 필요하다.
2) 경막외 자가혈액첩포(epidural blood patch)
경막외 자가혈액첩포(이하 혈액첩포)는 PDPH에서 오랫동안 사용되어 온 치료법으로 SIH에도 비교적 이른 시기부터 적용되어 왔으며 현재까지도 SIH 치료의 중심으로 자리 잡고 있다(Fig. 7-A) [41]. 혈액첩포의 치료 기전은 크게 두 가지로 설명된다. 첫째는 척추강 내 혈액 주입으로 인한 일시적인 용적 및 압력 증가 효과이고, 둘째는 주입된 혈액이 경막 결손 부위로 이동하여 직접적으로 누출 부위를 봉합(sealing)하는 효과이다.
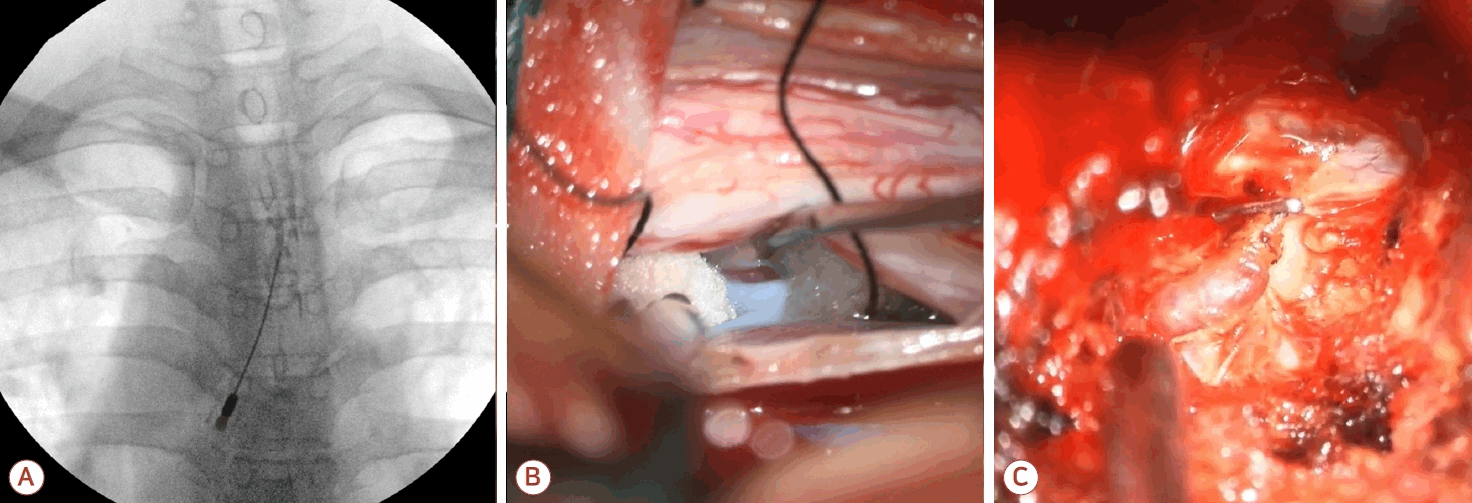
Treatment examples in spontaneous intracranial hypotension. (A) Targeted epidural blood patch in T2-3. (B) Intraoperative view of T1-2 ventral dural defect. (C) Intraoperative view of clipping of T12-L1 CSF-venous fistula. CSF; cerebrospinal fluid.
그러나 SIH에서의 혈액첩포는 PDPH에서의 혈액첩포와 여러 측면에서 차이를 보인다. PDPH에서는 누출 부위가 대개 요추부로 국한되는 반면 SIH에서는 누출 부위가 흉추 또는 경추를 포함하여 다양하게 분포할 수 있다. 또한 PDPH에서 시술 접근은 주로 경막의 후방(dorsal side)에서 이루어지지만 SIH에서는 실제 누출 부위는 전방(ventral, 1형)이나 측방(lateral, 2형)에 위치하는 경우가 많다. 이러한 해부학적 불일치는 SIH에서 혈액첩포의 효과를 제한하는 주요 요인 중 하나이다[43].
또한 3형 누출(뇌척수액-정맥 누공)과 같은 아형에서는 병태생리적으로 혈액첩포로 인한 누출 봉합이 불가능하며 효과가 있더라도 대개 수일(약 3-7일) 이내의 일시적인 호전에 그치는 경우가 많다. 따라서 이러한 아형에서는 혈액첩포에 대한 반응을 기대하기보다는 보다 근본적인 치료 전략을 고려해야 한다.
중요한 점은 혈액첩포가 단일한 치료 기법이 아니라 다양한 이질적 방법들이 포함된 치료군이라는 것이다[44]. 시술 위치에 따라 표적(targeted) 첩포와 비표적(non-targeted 또는 blind) 첩포로 나눌 수 있으며 단일 레벨(single-level) 또는 다중 레벨(multi-level) 시술, 자가혈액 단독 주입과 피브린(fibrin) 혼합 주입 등 다양한 변형이 존재한다. 또한 최근에는 기존의 추궁간접근(interlaminar approach) 외에도 추간공접근(transforaminal approach), CT 유도하에 SLEC 내 혈액첩포 등이 제안되고 있다[45]. 이러한 다양한 기법들을 직접 비교한 고품질 연구는 제한적이므로 단일한 방법만을 표준으로 제시하기는 어렵다. 그럼에도 불구하고 현재까지의 근거를 바탕으로 다음과 같은 일반적인 원칙을 제시할 수 있다.
첫째, 혈액첩포를 시행할 수 있는 환경이라면 가능한 한 조기에 시행하는 것이 바람직하다. 보존적 치료만으로 경과를 관찰하더라도 약 2주 이상의 보존적 치료에도 증상이 지속되는 경우에는 이후에도 호전 가능성이 낮으며, 이 경우 지체 없이 혈액 첩포를 시행하는 것이 권고된다[28].
둘째, 표적 혈액첩포는 비표적 혈액첩포보다 효과적이다. 그러나 누출 부위를 확인하기 위한 정밀 검사를 위해 치료가 과도하게 지연되는 경우라면 우선 비표적 혈액첩포를 시행하는 것이 합리적일 수 있다[41]. 비표적 혈액첩포는 접근이 용이한 요추부에서 시행되는 경우가 많으나 임상의의 판단에 따라 경추부나 흉추부에서 시행하거나 여러 레벨에서 시행할 수도 있다. 일반적으로 2회 이상의 비표적 혈액첩포에도 반응이 없는 경우에는 불응성으로 간주한다[28].
셋째, 상대적으로 많은 혈액량을 주입하는 것이 효과적이다. 메타분석에 따르면 대용량(>20 mL) 혈액첩포의 반응률은 77%로, 소용량(≤20 mL) 혈액첩포의 반응률(66%)보다 높게 보고되었다[27]. 다만 실제 임상에서는 환자의 통증으로 인하여 고용량 주입이 어려운 경우가 많다. 최근에는 절대적인 특정 값 이상의 용량 주입을 권고하기보다는 각 척추 레벨에서 혈액첩포가 유발하는 국소 압력 상승이 더 중요하다는 주장도 제기되고 있다[46]. 일반적으로 남성이 여성보다 약 3-4 mL 더 많은 용량을 견딜 수 있으며 하위 척추 레벨에 비해 상위 레벨에서는 주입 가능한 혈액량이 상대적으로 감소한다[47].
혈액첩포 이후에는 일반적으로 24-48시간의 침상 안정이 권고되며 일부 연구에서는 이를 더 연장할 것을 제안하기도 한다. 다만 이에 대한 근거는 제한적이며 임상 상황에 따라 조정된다.
3) 수술적 치료(surgical repair)
수술적 치료는 뇌척수액 누출 부위를 직접적으로 봉합하는 근치적 치료 방법이다. 수술적 치료의 적응증은 크게 세 가지로 나눌 수 있다. 첫째, 반복적인 혈액첩포에도 불구하고 증상이 지속되는 경우이다. 둘째, 해부학적 또는 병태생리적 이유로 혈액 첩포만으로 완치를 기대하기 어려운 경우이다. 대표적으로 3형 누출(뇌척수액-정맥 누공) 또는 장기간 지속되어 척추강 내 뇌척수액 저류가 구조화된 1형 누출이 이에 해당한다. 셋째, 진행성 경막하혈종이나 인지기능 저하, 보행장애를 동반한 표재철 침착증 등과 같이 SIH로 인한 합병증이 중증이어서 조기에 근치적 치료가 필요한 경우이다.
수술적 치료는 누출 부위의 정확한 국소화 이후 시행되어야 한다. 1형 및 2형 누출의 경우 일반적으로 후방 접근을 통해 결손 부위를 자가 근육이나 보강 물질을 이용해 봉합하며, 3형 누출의 경우 뇌척수액이 유입되는 정맥을 직접 결찰하거나 소작하는 방식으로 이루어진다(Fig. 7-B, C).
만성 경과를 보인 환자에서는 누출 부위 주변에 신생막 형성이나 유착이 동반되어 실제 누출 부위의 확인과 완전한 봉합이 어려운 경우가 있기 때문에 각별한 주의가 필요하다. 수술적 치료 후에는 대부분의 환자에서 두통과 기립 제한 증상이 또렷하게 호전되며 뇌MRI 및 척추MRI상 이상 소견 역시 점진적으로 정상화되는 경향을 보인다[44]. 다만 일부 환자(약 20%)에서는 수술 후 반동두개내압상승(rebound intracranial hypertension)이 지속되거나 영상학적으로는 호전을 보이더라도 임상 증상 중 일부가 장기간 지속되는 경우도 존재한다[48]. 이러한 특성을 고려할 때 수술적 치료의 계획과 수술 전후 환자 관리는 신경과, 신경외과, 영상의학과 전문의가 참여하는 다학제적 논의를 통해 이루어지는 것이 바람직하다.
4) 혈관 내 색전술(endovascular embolization)
최근 3형 누출(뇌척수액-정맥 누공)을 중심으로 혈관 내 색전술이 새로운 치료 옵션으로 제시되고 있다[49]. 이 치료법은 주로 정맥 경로를 통해 누공으로 연결된 배출 정맥을 색전시키는 방식으로 시행되며, 절개 수술을 시행하지 않고 병변을 차단할 수 있다는 점에서 상대적으로 침습도가 낮은 치료법으로 여겨진다. 특히 고령 환자이거나 전신 상태로 인해 수술적 접근의 부담이 큰 경우 혈관 내 치료는 유용한 대안이 될 수 있다.
4. 진단 및 치료 알고리즘 제안
본 종설에서는 SIH가 의심되는 환자에서 임상적 병력과 영상 소견을 단계적으로 통합하는 진단 및 치료 알고리즘을 제안한다(Fig. 8). 먼저 선행 외상이나 시술 없이 발생한 기립두통을 중심으로 SIH가 임상적으로 의심되는 경우 조영증강 뇌MRI와 척추MRI를 초기 영상 검사로 시행한다. 이는 SIH의 존재 여부를 확인함과 동시에 합병증을 평가하기 위한 필수적인 단계이다. 척추MRI에서 척추강 내 뇌척수액 저류가 확인되는 경우, 이는 SIH를 강력히 시사하며 1형 또는 2형 누출 가능성이 높다. 이러한 경우에는 비표적 혈액첩포를 우선 시행하고 반복 치료에도 반응하지 않는 경우 누출 부위 국소화를 위한 DSM 또는 동적 CT척수조영술을 고려한다[38]. 이후 누출 부위가 확인되면 표적 혈액첩포를 시행하거나 수술적 치료를 고려한다.
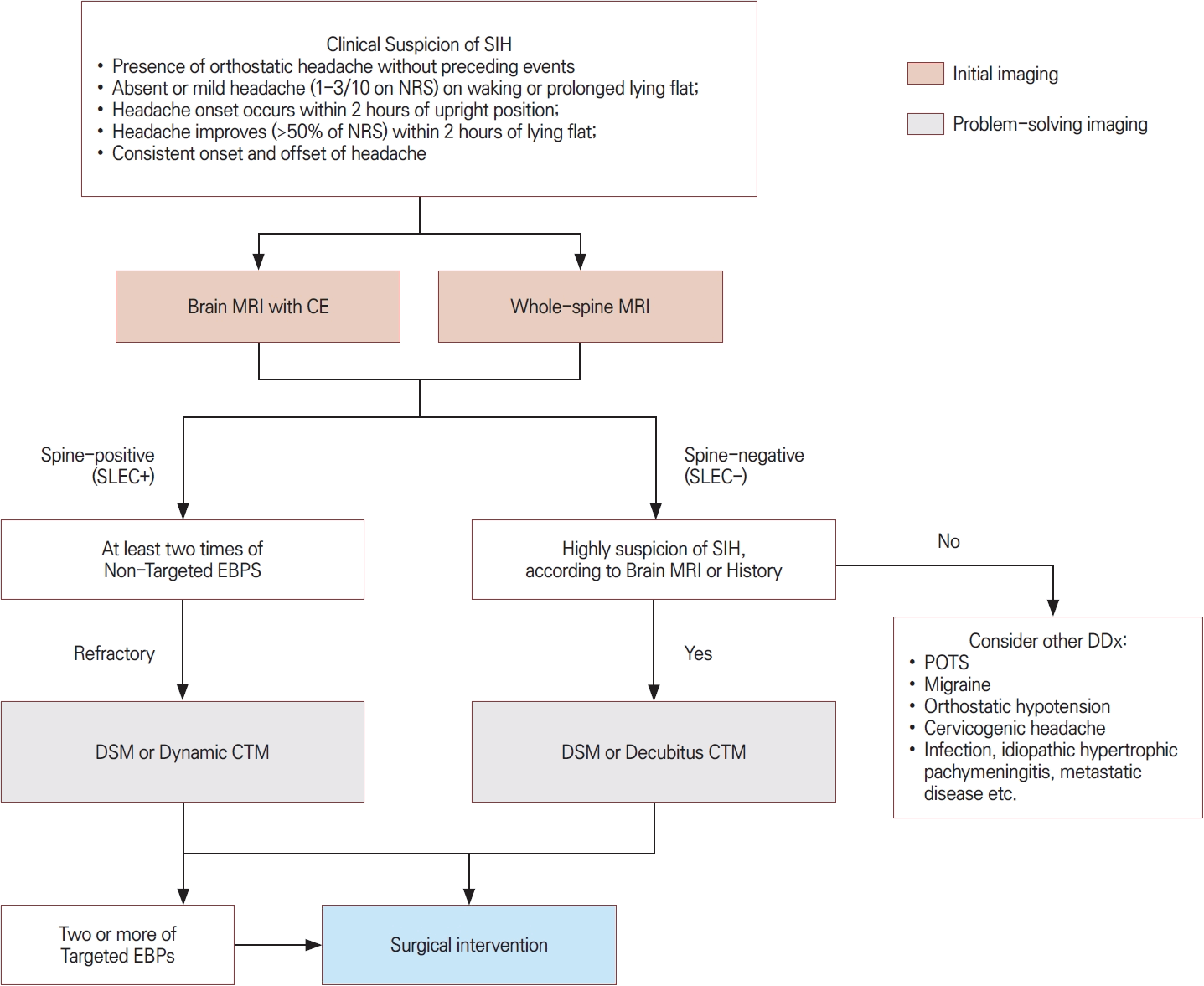
Proposed diagnostic and therapeutic algorithm for spontaneous intracranial hypotension. SIH; spontaneous intracranial hypotension, NRS; numerical rating scale, MRI; magnetic resonance imaging, CE; contrast enhancement, SLEC; spinal longitudinal epidural collection, EBP; epidural blood patch, DSM; digital subtraction myelography, CTM; computed tomography myelography, DDx; differential diagnosis, POTS; postural orthostatic tachycardia syndrome.
반면 척추MRI에서 뇌척수액 저류가 관찰되지 않는 경우에는 뇌MRI 소견과 병력을 바탕으로 SIH에 대한 임상적 의심도를 재평가한다. SIH 가능성이 낮다면 다른 기립두통의 원인에 대한 감별 진단을 진행하고, SIH가 여전히 강하게 의심되는 경우에는 DSM 또는 측와위 CT척수조영술을 통해 3형 누출의 가능성을 평가한다. 이러한 접근은 불필요한 침습적 검사를 최소화하면서도 치료 가능한 누출 병변을 놓치지 않기 위한 전략이다.
5. 한국에서의 현실적 제한점과 향후 과제
이와 같은 진단 및 치료 전략은 현재 SIH에 대한 이해와 국제적 진료 흐름을 반영한 것이나 국내 의료 환경에서는 여러 현실적인 제한점이 존재한다. 첫째, 현재 국내 요양 급여 기준에서는 SIH 진단을 목적으로 한 척추MRI, 특히 자기공명척수조영술(MR myelography)이 명확한 급여 항목으로 인정되지 않아 검사 시행에 제약이 있다. 이로 인하여 비급여 검사로 시행하거나 초기 단계에서 충분한 영상 평가가 이루어지지 못하는 경우가 적지 않다. 둘째, 척수조영술 자체는 고식적 검사로 급여 청구가 가능하나 최근 SIH 진단에서 핵심적인 역할을 하는 DSM이나 동적 CT척수조영술과 같은 동적 척수조영술 기법들은 아직 요양 급여 대상으로 정식 등록되어 있지 않다. 이로 인하여 해당 검사는 일부 기관에서 제한적으로 시행되는 경우가 많다. 셋째, 이러한 검사 및 치료 전략은 고도의 전문성과 장비와 다학제적 협력이 요구되므로 현재로서는 일부 의료기관 중심으로만 제한적으로 적용되고 있는 실정이다. 이는 SIH 환자의 진단 지연과 불필요한 반복 치료로 이어질 수 있다. 향후에는 SIH에 대한 질환 인식 제고와 함께 최신 진단 기법과 치료 전략이 국내 보험 제도와 진료 환경에 반영될 수 있도록 근거 축적과 제도적 논의가 필요하다. 이를 통해 SIH 환자들이 보다 적절한 시기에 정확한 진단과 치료를 받을 수 있는 진료 체계가 구축되어야 할 것이다.
결 론
SIH는 더 이상 드물거나 양성적인 경과를 보이는 질환으로만 인식되어서는 안 된다. 임상 양상이 다양하고 진단이 지연되는 경우가 많으며 적절한 치료 시기를 놓칠 경우 중증 합병증이나 만성적인 신경학적 후유증으로 이어질 수 있다. 따라서 SIH의 진단에서는 기립두통을 중심으로 한 병력 청취와 조영증강 뇌 MRI, 척추MRI를 포함한 영상 소견을 종합적으로 해석하는 접근이 필수적이다.
최근 SIH에 대한 이해는 뇌척수액 누출의 병인적 아형에 기반한 진단 및 치료 전략으로 발전하고 있다. 이에 따라 혈액첩포는 여전히 치료의 중심을 이루지만 누출 유형과 위치에 따른 표적 치료, 수술적 치료, 선택적인 혈관 내 치료의 역할이 점차 중요해지고 있다. 본 종설에서 제시한 진단 및 치료 알고리즘은 이러한 최신 개념을 임상 진료에 적용하기 위한 하나의 실용적인 틀을 제공하고자 하였다.
한편 국내에서는 SIH의 진단과 치료에 필수적인 일부 영상 기법과 치료 전략이 제도적 한계로 인하여 충분히 활용되지 못하고 있는 현실적인 문제가 존재한다. 향후 SIH에 대한 인식 제고와 함께 근거 축적 및 제도적 개선이 이루어진다면 보다 많은 환자들이 적절한 시기에 정확한 진단과 치료를 받을 수 있을 것으로 기대된다.
Notes
ACKNOWLEDGEMENTS
본 연구는 대한두통학회(Korean Headache Society)의 short-term fellowship의 지원을 받아 수행되었다. 본 종설에 포함된 영상 자료는 세브란스병원에서 시행된 검사 및 치료 증례를 기반으로 하였으며 종설 작성을 위한 학술적 사용에 대해 기관생명윤리위원회의 승인을 받았다(No. 4-2025-1621).

