특발 정상압수두증의 임상적 특징 및 진단적 접근의 최신 지견
Clinical Characteristics and Recent Advances in the Diagnostic Approach for Idiopathic Normal Pressure Hydrocephalus
Article information
Trans Abstract
Idiopathic normal pressure hydrocephalus (iNPH) is a potentially reversible neurological condition prevalent in the elderly, characterized by gait disturbance, cognitive decline, and urinary incontinence. Distinguishing iNPH from neurodegenerative mimics such as Alzheimer’s or Parkinson’s disease is critical to prevent missed treatment opportunities. This narrative review synthesizes current literature on the clinical presentation and diagnostic strategies for iNPH. Gait disturbance, often described as a magnetic gait, is typically the earliest sign and shows the most significant improvement following shunt surgery. Cognitive impairment manifests as frontal-subcortical dysfunction, distinct from the cortical memory deficits of Alzheimer’s disease. Diagnosis relies on integrating clinical history with specific magnetic resonance imaging findings, including disproportionately enlarged subarachnoid space hydrocephalus (DESH) and high-convexity tightness. While the cerebrospinal fluid (CSF) tap test is a valuable predictor for shunt responsiveness, clinicians must be wary of false-negative results. In addition, dopamine transporter imaging and amyloid imaging could be helpful to rule out other neurological disorders. Accurate diagnosis of iNPH requires a multidisciplinary approach combining clinical assessment, neuroimaging, and CSF dynamic evaluation. Timely identification and exclusion of comorbidities allow for effective surgical intervention, significantly reversing symptoms and improving the long-term quality of life for affected older adults.
정상압수두증(normal pressure hydrocephalus, NPH)은 Hakim과 Adams가 1965년에 처음 기술한 질환으로 보행장애, 인지기능 저하, 요실금의 세 가지 증상을 특징으로 한다[1]. 정상압수두증은 적절한 진단과 치료가 이루어질 경우 증상의 호전을 기대할 수 있는 대표적인 신경계 질환으로 그 임상적 중요성이 크다. 유병률은 연구에 따라 다양하나 고령에서 드물지 않게 발생하는 것으로 생각되는데, 일반적인 65세 이상의 인구에서는 약 0.5-2.9% 수준으로 보고되고 있으며 장기 요양 시설에 거주하는 노인 인구에서는 더 흔할 수 있다고 여겨지고 있다[2]. 하지만 정상압수두증 환자들은 노화로 인한 노쇠로 오인되거나 파킨슨병이나 알츠하이머병 같은 신경 퇴행 질환과 중첩되어 나타나는 경우가 많아 초기 진단이 쉽지 않다. 이러한 진단의 어려움 때문에 치료 가능한 시기를 놓칠 위험이 존재한다.
수두증을 논할 때 이차 수두증(뇌막염, 지주막하출혈, 외상 등 명확한 선행 원인 이후 발생하는 경우)과 60세 이후 특별한 선행 원인이 없이 발생하는 특발 정상압수두증(idiopathic normal pressure hydrocephalus)을 구분하는 것이 중요하다. 즉 이차성 사례는 별개이며 특발성 사례와 명확히 구분되어야 한다. 특발 정상압수두증은 그 원인이 아직 명확히 규명되지 않았거나 여러 요인이 복합적으로 작용하는 것으로 여겨지는 증후군이며, 이 증후군의 존재를 부정하는 것은 삶의 질에 중요한 영향을 미칠 수 있는 질환의 치료 기회를 환자에게서 박탈하는 위험을 내포한다. 일부에서는 정상압수두증의 실체에 대해 의문을 제기해 왔으나 실제 임상 진료 현장에서는 정상압수두증이 실제로 존재하는 질환이라는 것이 분명하다[3]. 반면 특발 정상압수두증에 대한 명확한 임상적인 이해가 부족하면 자칫 과잉 진단으로 이어질 수 있고 이로 인하여 부적절한 신경외과적 치료가 시행되는 경우도 있을 수 있어 주의가 필요하다. 본 종설에서는 이차 수두증을 제외하고 특발 정상압수두증에 한정하여 논의하기로 하겠다.
최근 정상압수두증의 병태 생리에 대해 잘 정리된 논문이 있어 대한민국의 임상가들 및 연구자들이 정상압수두증을 이해하는 데 많은 도움을 주고 있다[4]. 추가적으로 정상압수두증의 다양한 임상 증상에 대한 체계적인 고찰과 임상적 진단에 대한 최신 지견이 잘 정리된다면 정상압수두증의 정확한 진단과 적절한 치료 전략 수립에 실질적인 도움이 될 것으로 사료된다. 특히 최근에 고해상도 뇌자기공명영상(magnetic resonance imaging, MRI), 뇌척수액(cerebrospinal fluid, CSF) 검사, 다양한 생물표지자 분석 등 진단 방법의 발전과 국제 진료지침의 도입으로 정상압수두증의 진단의 정확도와 치료 성적이 크게 향상되었다. 이에 본 종설에서는 최신 문헌을 바탕으로 정상압수두증의 임상 양상과 진단 방법을 서술적 고찰을 통해 체계적으로 정리하고자 한다.
본 론
1. 정상압수두증을 시사하는 임상 양상과 특징
정상압수두증의 임상 양상은 고전적으로 보행장애, 인지기능 저하, 배뇨장애의 3대 증상(triad)으로 구성된다[5]. 그러나 실제 임상에서는 이들 증상이 모두 동시에 나타나는 경우는 드무며 보행장애가 가장 먼저, 가장 뚜렷하게 발현되는 경우가 많다.
1) 보행장애
정상압수두증에서 보행장애(gait disturbance)는 질환을 의심하게 하는 가장 뚜렷한 초기 증상이지만 보행의 양상은 환자들마다 다양할 수 있다. 주로 고위기능보행장애(higher level gait disorder)의 패턴을 보이나 일부에서 중간기능보행장애(middle level gait disorder)의 특징을 함께 보일 수 있기 때문이다[5,6]. 많은 환자들은 초기에는 ‘발이 땅에 붙어있는 느낌,’ ‘걷기 시작이 힘듦’과 같은 비특이적인 보행 불편감을 먼저 호소한다. 이후 증상이 진행됨에 따라 양발을 넓게 벌리면서(wided-based) 작은 보폭으로 양발을 끄는 듯한 양상의 소위 자석 보행(magnetic gait)이 나타난다. 일부 환자들에서는 전형적인 동결 보행(freezing gait) 없이 상당한 자세불안정성(postural instability)을 동반한 보행 불균형(gait imbalance)이 나타날 수 있으며 이로 인하여 평형장애(disequilibrium)와 잦은 낙상을 경험하게 된다[7]. 또한 어떤 환자들은 파킨슨병과 유사한 보행 양상을 보이기도 하여 임상적으로 파킨슨병과의 감별이 어려운 경우도 있다[8]. 즉 정상압수두증에서는 다양한 보행 양상을 보일 수 있으므로 단순히 보행 양상만으로 진단을 내리기보다는 다양한 질환에 대한 감별 진단이 필요하다.
정상압수두증과 파킨슨병의 보행 양상은 차이가 있으나 일부 유사한 특징을 공유하여 임상적으로 구분이 어려울 수 있다. 정상압수두증의 전형적인 보행의 양상은 보행 속도가 느려지면서 넓은 보폭에 불규칙한 걸음을 보이는데, 일부에서는 주춤거림을 보이는 동결 보행(freezing gait)과 방향 전환 시 여러 단계에 걸쳐 천천히 돌게 되는 통나무 회전(en bloc turning)을 보인다[9]. 반면 파킨슨병에서는 보행 속도의 저하와 함께 보폭이 좁아지면서 종종걸음이 나타나는 것이 특징적이며 동결 보행(freezing gait)은 일반적으로 질환이 상당히 진행된 이후에 발생하는 경향이 있다[10].
보행장애는 정상압수두증의 여러 임상 증상들 중에서 초기 증상일 뿐만 아니라 수술에 대한 효과가 우수한 것으로 알려져 있다. 대표적으로 다기관이 참여한 유럽의 연구에서 115명의 환자를 대상으로 분석한 결과 션트(shunt) 수술 후 약 84%의 환자에서 보행 점수의 유의미한 향상이 확인되었다[11]. 또한 최근 메타 분석 연구에서는 수술 후에 약 72%의 환자에서 보행기능의 개선이 보고되었다[12]. 반면 다른 연구에서 수술을 하지 않은 환자들에서는 보행의 악화가 관찰되며 주로 보행과 균형능력이 점차 악화되는 경향이 관찰된다[13]. 수술을 거부한 정상압수두증 추정 환자 9명을 추적 관찰한 결과 보행장애가 악화된 비율이 12개월 후 33%에서 24개월 후 89%로 급격히 증가하였다는 보고도 있다[14]. 또한 수술 없이 수년간 추적 관찰한 다른 환자군(26명)에서도 1년 후에 63%, 5년 후에는 65%에서 보행장애가 지속되거나 악화된 것으로 보고되었다[15].
2) 인지기능 저하
정상압수두증 환자에서 관찰되는 인지기능 저하는 주로 전두엽-피질하기능장애(frontal-subcortical dysfunction)의 양상을 보이며 이는 알츠하이머병과는 구별되는 중요한 특징이다[5]. 환자들은 주로 주의력 결핍, 정신운동 속도(psychomotor speed)의 감소, 기억력 감퇴를 흔히 경험하는데, 이때의 기억력 저하는 알츠하이머병과 달리 재인 단서(recognition cues)를 통해 회상 능력이 보완되는 피질하기억장애 패턴을 보인다[16]. 인지기능 저하의 정도는 경도인지장애부터 진행성 치매에 이르기까지 다양하며 질병의 기간이나 환자의 연령에 따라 차이를 보일 수 있다. 특히 무감동(apathy)이 흔하게 동반되며 초기에는 집행기능(executive function)의 저하가 두드러지다가 점차 광범위한 인지기능 저하로 진행되는 경향이 있다[17,18].
션트(shunt) 수술은 이러한 인지기능 저하, 특히 학습능력, 기억력, 정신운동 속도를 개선하는 데 효과적일 수 있다[19]. 많은 연구에서 간이정신상태 검사(mini-mental state examination, MMSE)나 몬트리올 인지평가(Montreal cognitive assessment, MoCA)와 같은 선별 검사가 사용되지만 정상압수두증에서 특정한 단일 인지 영역을 정의하기는 어려우며, 환자마다 인지기능 증상의 이질성이 큰 것으로 알려져 있다. 최근한 메타 분석 연구에서는 수술을 시행할 경우 인지기능 저하는 대략 50% 호전된다고 보고하였다[12]. 다만 만약 보행장애보다 인지기능 저하가 먼저 나타나거나 실어증(aphasia)과 같은 국소 피질 증상이 동반되는 경우에는 정상압수두증 이외의 다른 원인을 우선적으로 고려할 필요가 있기 때문에 주의해야 한다[10].
3) 배뇨장애
정상압수두증 환자에서 나타나는 배뇨장애는 빈뇨, 절박뇨(urgency), 야간뇨(nocturia)와 같은 가벼운 증상에서부터 환자가 인지하지 못하는 요실금까지 다양한 범위로 나타날 수 있다. 일반적으로 절박뇨나 빈뇨와 같은 배뇨근 과다활동(detrusor overactivity) 증상이 먼저 나타나고 병이 진행됨에 따라 말기에는 요실금으로 이어지는 경향이 있다[5]. 요실금은 환자의 일상생활과 삶의 질에 큰 영향을 미치며 환자 본인은 물론 가족에게도 상당한 부담을 초래한다. 요역동학 검사에서 정상압수두증 환자의 다수가 배뇨근 과다활동을 보였으며 이는 뇌 영상 연구에서 관찰되는 우측 전두엽의 혈류 저하와 관련이 있어 배뇨반사의 억제 기능이 상실된 결과로 해석되기도 한다[20].
임상적으로 배뇨장애는 보행장애나 인지기능 저하에 비해 덜 중요하게 여겨지기도 하지만 실제로는 환자의 삶의 질에 인지기능 저하보다 더 부정적 영향을 미치는 경우가 많다. 다만 고령의 환자군 특성상 전립샘비대증이나 골반저근육 약화와 같은 다른 비뇨기계 질환이 공존할 가능성이 높으므로 모든 배뇨 증상을 정상압수두증에 의한 것으로 단정해서는 안되며 정확한 감별 진단이 필요하다[5]. 션트(shunt) 수술 후 배뇨기능의 호전을 기대할 수 있으나 증상의 진행 정도와 동반 질환 여부에 따라 치료 반응에는 차이가 있을 수 있다. 최근 메타 분석 연구에서는 수술 후 대략 50%의 환자에서 증상의 호전이 관찰된 것으로 보고되었다[12].
4) 기타 신경계 소견 및 감별점
정상압수두증의 임상 증상은 고령자에서 흔한 파킨슨병, 혈관 치매, 알츠하이머병뿐 아니라 전정기능 저하, 약물 부작용 등 다양한 원인과 중복될 수 있으므로 병력 청취와 임상적, 신체 소견, 신경계 진찰, 영상 검사를 포함한 객관적 평가를 종합하여 신중하게 진단하여야 한다. 또한 정상압수두증에서는 일반적으로 근력 저하, 감각 저하, 반사 이상 등 상부/하부 운동신경계 이상 소견은 동반되지 않는다. 따라서 이러한 신경계 이상 소견이 동반된다면 정상압수두증만으로 설명하기보다는 경추증(cervical spondylosis)이나 다발신경병증(polyneuropathy) 등을 비롯한 다양한 동반 질환의 가능성을 염두하고 추가적인 검사나 평가가 필요하다.
2. 정상압수두증을 진단하기 위한 검사와 유의점
정상압수두증의 진단에서 가장 중요한 것은 임상 증상과 영상 소견을 종합적으로 평가하는 것이다. 환자 선별의 적절성과 신중한 평가가 수술 예후와 직결되므로 다학제적 접근이 권장된다. 정상압수두증의 국제적 진단 지침에서는 임상 증상, 영상 소견, 보조 검사 결과를 바탕으로 진단 단계를 구분한다. 일본수두증학회에서는 definite (확실한), probable (유력한), possible (가능한) 단계로 분류하고 있으며[21] 세계수두증학회에서는 probable (유력한), possible (가능한), unlikely (불확실한) 단계로 진단 범주를 제시하고 있다[22]. 한편 미국신경학회(American Academy of Neurology, AAN)는 임상 진료지침을 통해 션트(shunt) 수술이 효과적일 수 있다는 결론을 제시하였으며, 뇌척수액에 대한 천자 검사(tap test) 또는 요추배액술(lumbar drainage)에 대한 양성 반응이 수술 효과를 예측하는 데 도움이 된다고 권고하였다[23].
1) 뇌영상
정상압수두증의 진단에서 영상 소견은 매우 중요하며 진단과 치료 과정에서 반드시 임상 증상과의 연관성을 함께 고려해야 한다. 뇌전산화단층촬영(computed tomography, CT)도 도움이 되지만 뇌의 구조적인 변화를 보다 정밀하게 평가할 수 있는 뇌MRI가 정상압수두증의 진단과 감별에 있어 더욱 유용하다[5,21,24,25]. 특히 뇌MRI는 정상압수두증을 시사하는 특징적인 소견들을 확인할 수 있을 뿐만 아니라 심한 허혈 변화, 뇌종양 또는 뇌 위축에 의한 이차 수두증 등 다른 원인 감별에 중요한 역할을 한다. 단순히 Evans index의 증가로 인한 뇌실 확장(ventriculomegaly)만으로는 진단적 가치가 충분하지 않음에 유의해야 한다. 뇌MRI를 확인할 때 정상압수두증에서 보이는 특징적인 소견들인 대뇌 궁륭부(볼록면)의 좁아짐(대뇌 위쪽 주름이 눌려 좁아지는 현상, cerebral convexity tightness), 뇌실 주위의 사이질부종(interstitial edema), 뇌량각의 좁아짐(callosal angle narrowing), 불균형 뇌지주막하공간 확장(disproportionately enlarged subarachnoid space hydrocephalus, DESH)의 유무를 종합적으로 평가하는 것이 중요하다(Fig. 1).
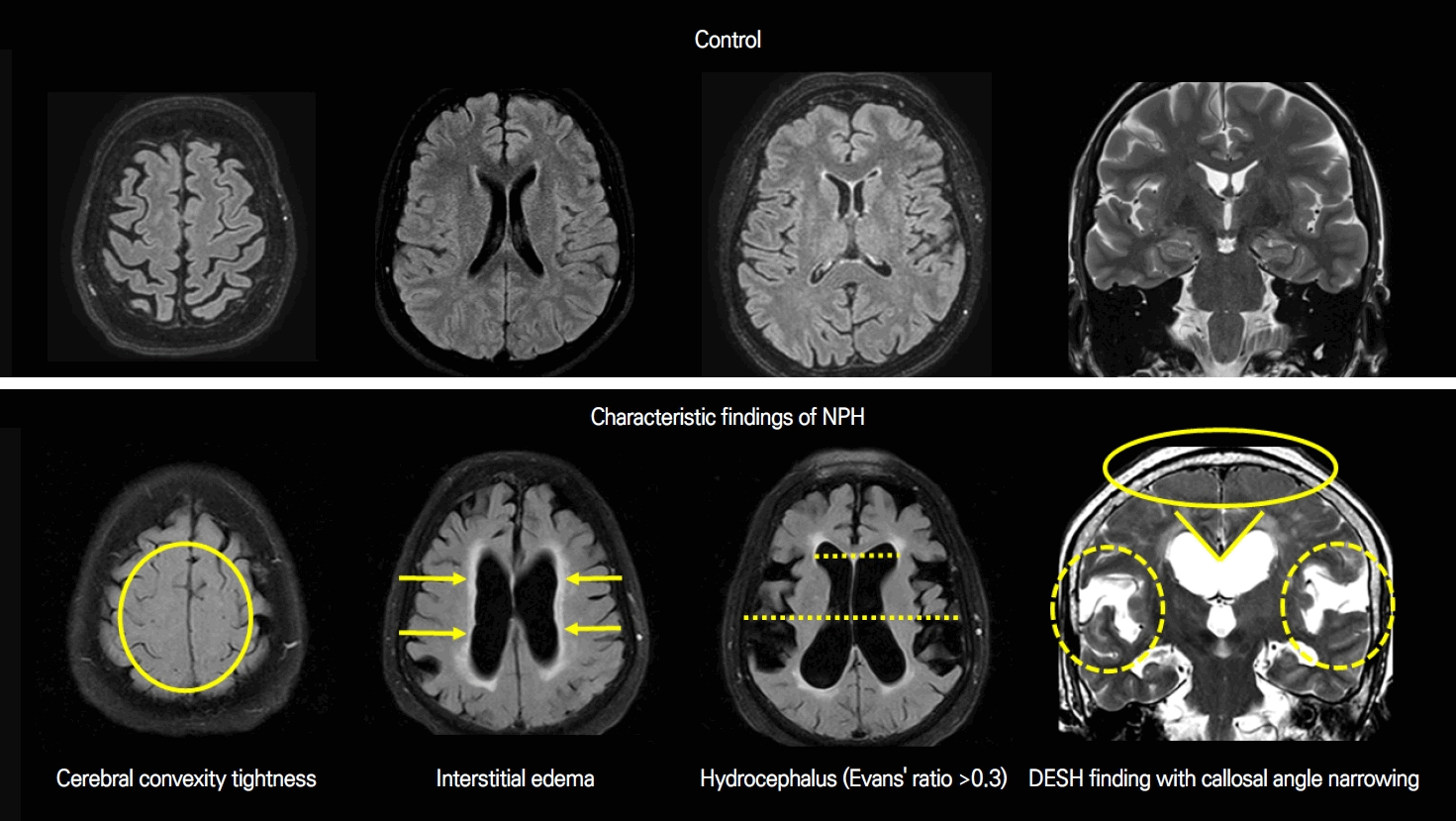
Representative brain MRI findings of idiopathic NPH. NPH; normal pressure hydrocephalus, DESH; disproportionately enlarged subarachnoid space hydrocephalus, MRI; magnetic resonance imaging.
또한 추가적인 뇌영상 검사들이 정상압수두증의 감별에 도움이 될 수 있다. 특히 보행장애를 주 증상으로 하는 파킨슨병이나 인지기능 저하를 보이는 알츠하이머 치매와 같은 질환에 대한 감별은 임상적으로 중요하다. 이러한 감별을 위하여 도파민운반체뇌영상(dopamine transporter imaging)과 아밀로이드뇌영상(amyloid imaging)의 시행은 정상압수두증에 동반된 다른 신경 퇴행 질환을 확인하거나 배제하는 데 있어 임상적으로 유용한 정보를 제공할 수 있다[25]. 정상압수두증 환자에서 도파민운반체영상(dopamine transporter imaging)을 분석한 결과 도파민 감소는 대체로 경미하고 조가비핵(putamen)보다 꼬리핵(caudate nucleus)에서 더 빈번하게 나타나는 경향이 있어 파킨슨병과는 다른 양상의 도파민 손실의 패턴을 보이므로 감별에 주의해야 한다[26]. 또한 아밀로이드영상(amyloid imaging)을 통해 인지기능 저하의 원인이 단순히 정상압수두증 때문인지 혹은 알츠하이머병과 같은 동반 질환이 영향을 끼치는지 보다 정확하게 확인할 수 있다[27]. 즉 아밀로이드영상(amyloid imaging)의 결과를 토대로 향후 션트(shunt) 수술을 시행하였을 때 인지기능의 호전 여부나 정도를 예측하는 데 중요한 힌트를 제공하게 된다. 특히 이와 같은 분자영상(molecular imaging)을 통한 공존 질환의 감별은 뇌척수액 천자 검사(CSF tap test)를 시행하기 어렵거나 검사 후에 명확한 임상 증상의 호전이 없는 환자에서 치료적 방침을 결정하는 데 있어 유용한 정보를 제공하므로 적극적으로 고려할 필요가 있다.
2) 뇌척수액 천자 검사
뇌척수액은 뇌실의 맥락총(choroid plexus)에서 만들어져 뇌실과 지주막하공간을 순환한 뒤 지주막과립(arachnoid granulations)을 통해 혈류로 다시 흡수된다. 사람마다 차이가 있지만 평균적으로 뇌척수액의 양은 150 mL 정도이며 노인에서는 뇌 수축에 의해서 350 mL까지 증가할 수 있다. 하루에 400-600 mL의 뇌척수액이 만들어지기 때문에 하루 기준으로 대략 3-4회 정도 순환하게 된다[28,29]. 자세한 뇌척수액의 병태 생리에 대하여는 최근 게재된 종설을 참조하는 것이 도움이 될 것이다[4].
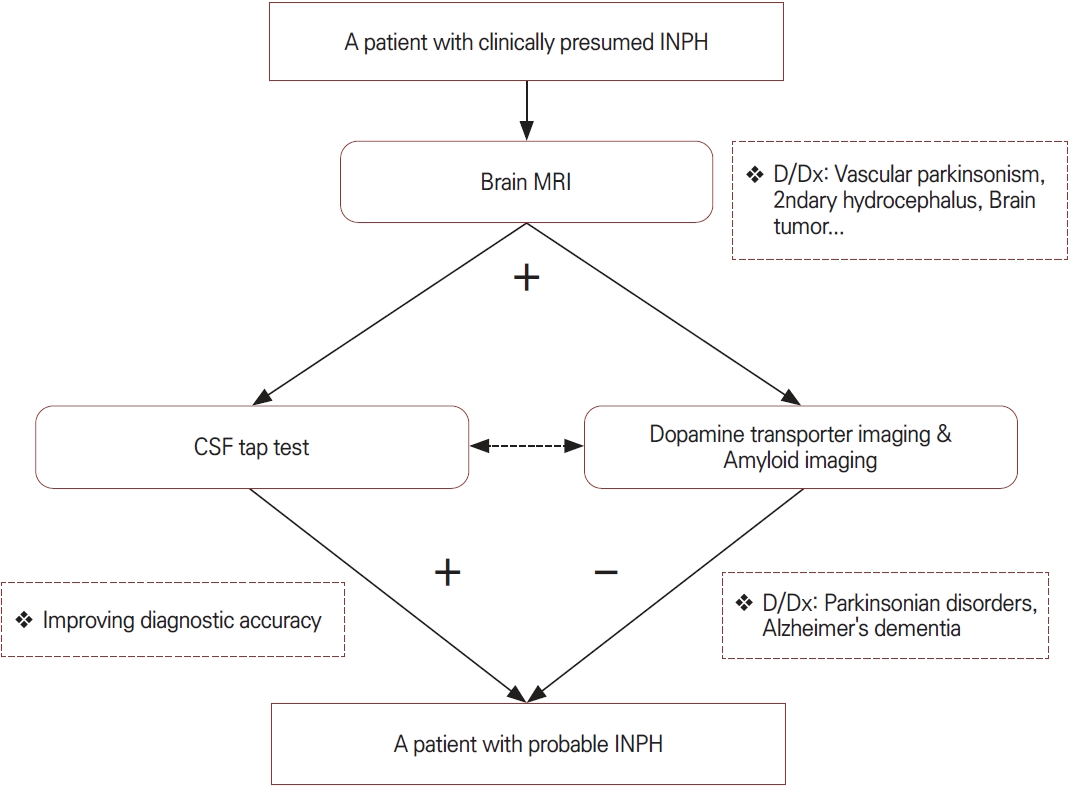
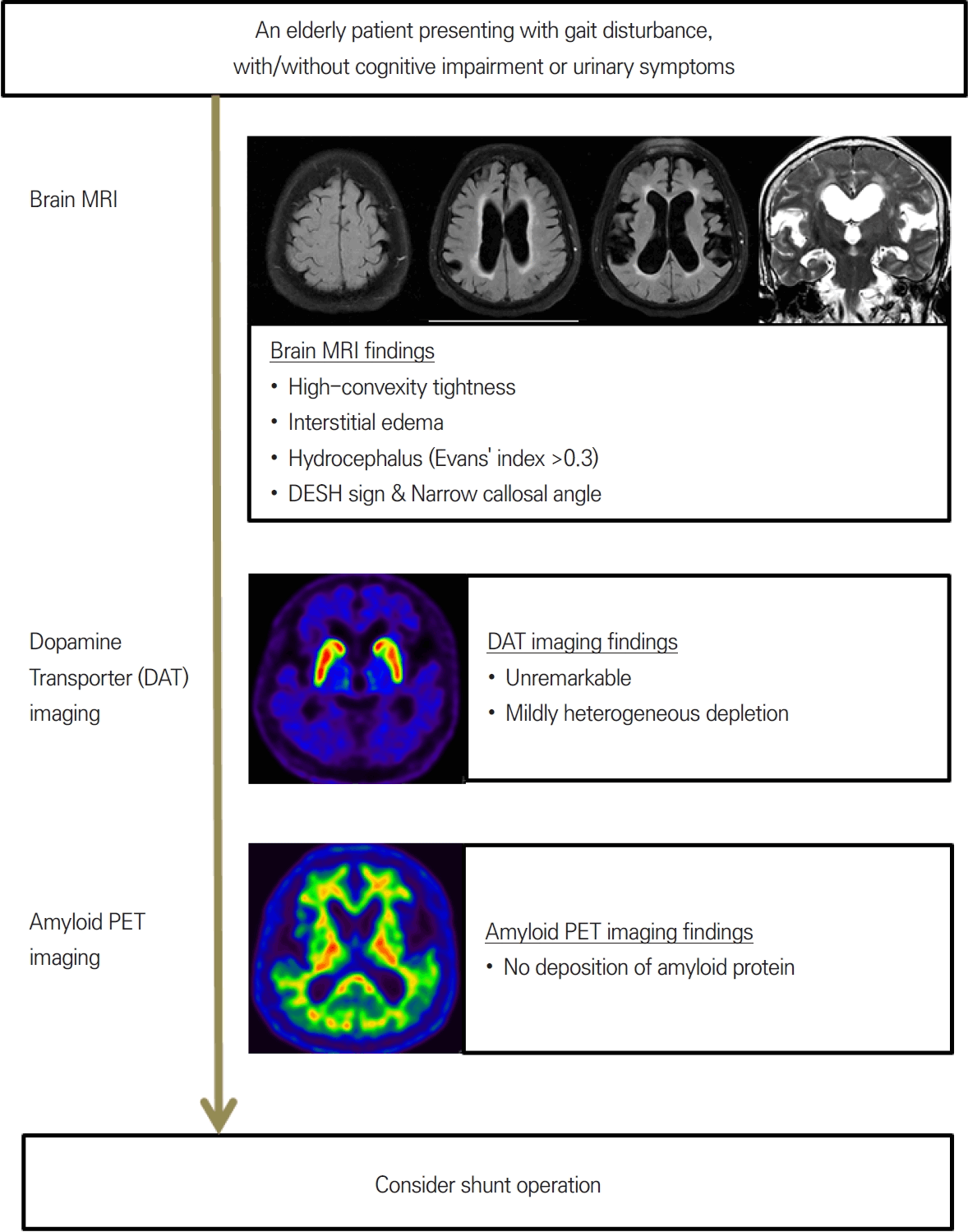
정상압수두증의 진단에서 뇌척수액 천자 검사(CSF tap test)는 요추천자를 통해 약 30-50 mL의 뇌척수액을 일시적으로 제거한 후 환자의 증상 개선 여부를 평가하는 중요한 진단 방법이다[10,21]. 또한 임상적인 필요에 따라서 여러 번 반복적으로 천자 배액을 시도하거나 1-3일간 지속적인 배액을 시도하여 증상의 호전을 평가할 수도 있다. 객관적인 보행 검사들(GAITRite를 이용한 보행 분석, timed up and go test, 10-meter walk) 및 주관적 증상 변화의 관찰을 통해 증상의 호전이 확인되면 향후 션트 수술(shunt surgery)로 호전될 가능성이 높은 환자를 선별할 수 있고 예후를 예측할 수 있다. 일본 진료지침에서는 뇌척수액 천자 검사 후 timed up and go test에서 10% 이상의 호전이 있을 경우를 양성으로 간주하고 있다[28,30]. 하지만 뇌척수액 천자 검사가 예민한 검사임에도 불구하고 위음성 가능성이 상당하므로 결과 해석에는 주의가 필요하다[10]. 한 연구에서는 양성 예측도(positive predictive value)는 최대 100%에 달하지만 음성 예측도(negative predictive value)는 최저 36%로 낮을 수 있다고 보고하였다[31]. 다른 연구에서는 뇌척수액 천자 검사 단독이 아니라 뇌량각의 좁아짐(callosal angle narrowing)과 DESH라는 영상 소견을 함께 고려하면 정상압수두증의 진단 정확도를 높이는 데 도움이 되는 것을 보여주었다[32]. 따라서 증상과 뇌MRI 소견이 모두 정상압수두증을 시사한다면 비록 뇌척수액 천자 검사에서 임상적 호전이 명확하지 않더라도 정상압수두증에 대하여 션트 수술의 가능성을 배제하지 말아야 할 것이다. 그렇기 때문에 증상에 대한 정확도를 높이기 위하여 뇌척수액 천자 검사의 결과에 의존하기보다는 오히려 추가적인 검사들을 통해 다른 질환들을 배제하는 접근이 상당히 유용할 수 있다(Fig. 2). 특히 앞서 언급한 분자영상(molecular imaging)을 통해 파킨슨병과 알츠하이머 치매와 같은 다른 주요 질환들에 대한 배제가 가능하다면 션트 수술을 적극적으로 고려해 볼 필요가 있을 것이다(Fig. 3).
3) 뇌척수액 생물표지자
뇌척수액 생물표지자(CSF biomarkers)는 알츠하이머병과 파킨슨병을 비롯한 신경 퇴행 질환의 평가에서 활발히 연구되고 있다. 그러나 정상압수두증에서 이러한 생물표지자의 임상 적용은 다소 더디게 진행되어 왔는데, 이는 뇌척수액의 역학적 특성 변화(분포 용적 증가, 글림프 흐름 이상, CSF 회전율 변화 등)가 비정상 단백질 농도에 영향을 미쳐 해석을 어렵게 만들기 때문이다[33]. 두 개의 체계적 문헌 고찰에 따르면 아밀로이드(amyloid)-β 42 (Aβ42), 총 타우(total tau), 인산화 타우(phosphorylated tau, p-tau), 신경섬유경쇄(neurofilament light chain), 류신 풍부 α-2당단백질(leucine-rich α-2-glycoprotein) 등이 정상압수두증과 알츠하이머병을 감별하고 션트(shunt) 수술에 대한 반응성을 예측하는 데 도움이 될 수 있다고 보고되었다[34,35]. 알츠하이머병에서는 일반적으로 p-tau 대비 Aβ42 비율의 증가가 특징적으로 나타나는 반면 정상압수두증처럼 뇌척수액 역학(CSF dynamics)이 변형된 상태에서는 Aβ42가 비정상적으로 감소하면서도 p-tau는 정상 범위를 유지하는 다른 양상을 보일 수 있다. 현재로서는 이러한 생물표지자(amyloid-β, p-tau, neurofilament light chain)는 정상압수두증의 진단에서 최근 연구를 통해 그 유용성이 탐색되고 있다. 향후에 다른 신경 퇴행 질환이나 동반 질환 가능성을 배제하는 데 유용성이 입증된다면 이를 통해 션트 수술 후 장기적인 보행 기능 호전 여부를 예측하는 데 활용할 수 있을 것이다.
4) 정상압수두증 진단에 있어서의 한계
임상의 입장에서 정상압수두증 환자의 션트 수술 여부를 결정할 때에는 양호한 예후가 기대되는 적응증과 함께 예후 예측의 본질적인 한계 및 불확실성을 다각적으로 고려해야 한다. 실제 한 전향적 관찰 연구에서는 전형적인 증상이 뚜렷하고 뇌 MRI에서 정상압수두증의 특징이 확인되고 뇌척수액 배액 검사에서 호전을 보였던 환자들에서 션트 수술 후 평균 5개월의 추적 후에 73%에서 증상이 호전됨을 보고하였다[36]. 또한 3-5년간의 장기간 추적 관찰에서는 정상압수두증 환자들이 수술 후에 지속적인 호전을 보이는 경우는 21-80%로 다양하게 보고되고 있다[37]. 따라서 환자의 동반 질환 상태, 수술로 인한 득실, 잠재적 합병증 위험, 실질적인 삶의 질 개선 효과를 종합적으로 저울질하여 신중하게 수술을 결정해야 한다.
결 론
정상압수두증은 적절하게 진단될 경우 치료가 가능할 수 있는 질환으로 노년층에서 보행장애, 인지기능 저하, 요실금 증상들의 조합 및 뇌영상 소견을 바탕으로 신속하고 정확한 평가가 필요하다. 임상 증상, 뇌MRI의 특징적인 소견, 분자영상(molecular imaging)의 활용, 뇌척수액 천자 검사(CSF tap test), 뇌척수액 생물표지자(CSF biomarkers) 등 다양한 진단 도구를 통합적으로 활용하고 신중하게 환자를 선별하는 것이 장기 예후 개선에 있어 매우 중요하다. 향후 유전자 및 생물표지자 연구, 새로운 신경영상 기술 발전 등을 통해 더 효과적인 정상압수두증의 진단 및 치료 전략이 개발될 것으로 기대한다.