저나트륨혈증 발생과 연관되어 증상 악화를 보이는 항LGI-1항체뇌염
Anti-LGI-1 Encephalitis with Worsening Symptoms Associated with Hyponatremia
Article information
Trans Abstract
Anti-leucine-rich glioma-inactivated 1 (LGI-1) encephalitis is clinically characterized by subacute cognitive decline and frequent seizures including fasciobrachial dystonic seizures. A 67-year-old man visited the emergency department due to the recurrent episodes of seizures of 4 days duration. At the time of the visit, he showed hyponatremia at Na 121 mg/dL. His symptoms were relieved by 3% sodium chloride and water restriction. Here we report a case of anti-LGI-1 encephalitis with worsening symptoms associated with hyponatremia.
자가면역뇌염은 세포내 존재하는 단백질에 대하여 항체를 가지는 경우(onconeuronal antibody)와 세포 표면에 있는 수용체나 신경연접부위의 단백질에 항체를 가지는 경우(antibodies targeting cell surface neuronal receptors or synaptic-proteins)로 나눌 수 있는데 항leucine-rich glioma-inactivated protein 1 (LGI-1)항체뇌염은 후 자에 해당되며 voltage gated pottasium channel (VGKC) network 중 일부의 문제이다[1]. LGI-1단백은 주로 해마와 측두엽의 신경연접 부위 사이공간(synaptic space)에서 분비되는데, 항LGI-1항체뇌염은 발작(seizure), 심한 기억력장애를 포함한 인지장애 그리고 행동이상이 주증상이다[2]. 항LGI-1항체뇌염 환자를 진단하였을 때 약 90%에서 발작이 있었으며 70-75%에서 저나트륨혈증이 있었다고 한다[3]. 항LGI-1항체뇌염에서 저나트륨혈증의 원인은 시상하부의 뇌실곁핵(paraventricular nucleus of hypothalamus)에 항체가 붙어서 부적절 항이뇨호르몬분비증후군(syndrome of inappropriate antidiuresis, SIADH)을 유발하는 것으로 사료된다[4]. 저자들은 항LGI-1항체뇌염에서 저나트륨혈증의 발생과 이에 따른 경련의 악화 그리고 면역억제 치료와 전해질 교정 치료에 의한 경련의 완화를 경험하여 이를 보고한다.
증 례
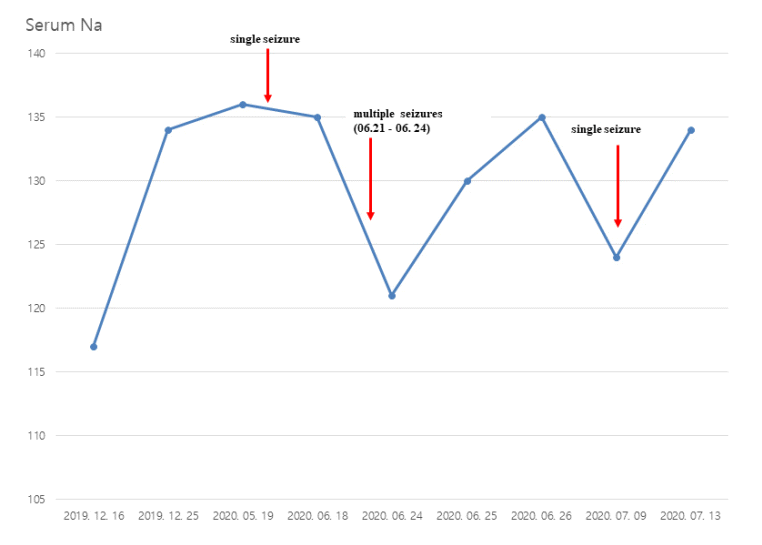
67세 남자가 비교적 급격히 악화되는 기억력장애로 왔다. 당시 혈액화학검사에서 Na 117 mg/dL로 저나트륨혈증 소견을 보였고, 혈청오스몰랄농도 243 mOsm/kg, 뇨오스몰랄농도 419 mOsm/kg, 소변 Na 40 mg/dL로 측정되어 부적절항이뇨호르몬분비증후군(SIADH)으로 내분비내과에 입원하였다. 당시 발작은 없었고 3% NaCl 수액을 주사 후 수일내 정상화되었다(Fig. 1). 과거력 상 간헐적인 음주력이 있었고 고혈압과 당뇨가 있어 이에 대하여 투약 중이었다. 환자는 9년 학력이었으며 2020년 1월 시행된 서울신경심리선별종합검사(Seoul Neuropsychological Screening Battery, SNSB)에서 기억력, 전두엽기능 그리고 시공간 인지기능의 저하 소견과 이로 인한 일상생활능력의 감소를 보이는 임상치매평가척도(clinical dementia rating scale, CDR) 1단계 치매 상태였다. 간이정신상태검사 18점이고 CDR-SOB 9점이었다. SNSB-dementia version (SNSB-D)의 종합점수(composite score)는 112점이었다(Fig. 2). 뇌 magnetic resonance imaging에서 양쪽 뇌의 내측 관자엽부위(특히, 좌측 편도체와 해마)의 광범위한 백질고신호강도(white matter hyperintensities, WMHs)를 보였고(Fig. 3), 뇌척수액검사에서는 뇌척수액압 15 cmH2O, 백혈구는 7/μL, 적혈구는 0/μL, 단백질은 89.0 mg/dL였으며 혈청 및 뇌척수액에서 항LGI-1항체가 발견되어 항LGI-1항체뇌염으로 진단되었다. 뇌척수액을 사용한 자가면역뇌염 시냅스항체검사(autoimmune synaptic encephalitis antibody)에서 항NMDA, 항AMPA, 항 CASPR2, 항DPPX, 항GABA-B항체와 항신생물딸림증후군항체(paraneoplastic auto antibody)인 항Hu, 항Yo, 항Ri, 항amphiphysin, 항CV2, 항PNMA2, 항Recoverin, 항SOX1, 항Titin항체는 모두 음성이었다. 뇌척수액 그람염색, 세균배양검사, AFB 형광염색과 배양 검사에서 모두 음성이었으며 CSF-아데노신탈아미노효소는 5 IU/L로 측정되었다. 환자는 여러 차례 입원하여 스테로이드 충격요법(steroid pulse therapy), 5일간의 면역글로불린 정맥주사(intravenous immunoglobulin, IVIG), 리툭시맙(rituximab) 4주 치료 그리고 토실리 주맙(tocilizumab) 8 mg/kg 주사 1회 치료를 받았다. 본 환자에서 면역글로불린과 rituximab의 치료는 경미한 인지기능의 호전을 보였으나(SNSB-D score 116점에서 132점으로 증가, Fig. 2) 일시적이었으며 tocilizumab은 첫 주사 이후 뚜렷한 효과가 없어서 중단되었다.

Changes in SNSB-D scores over time. SNSB-D; Seoul Neuropsychological Screening Battery-dementia version.
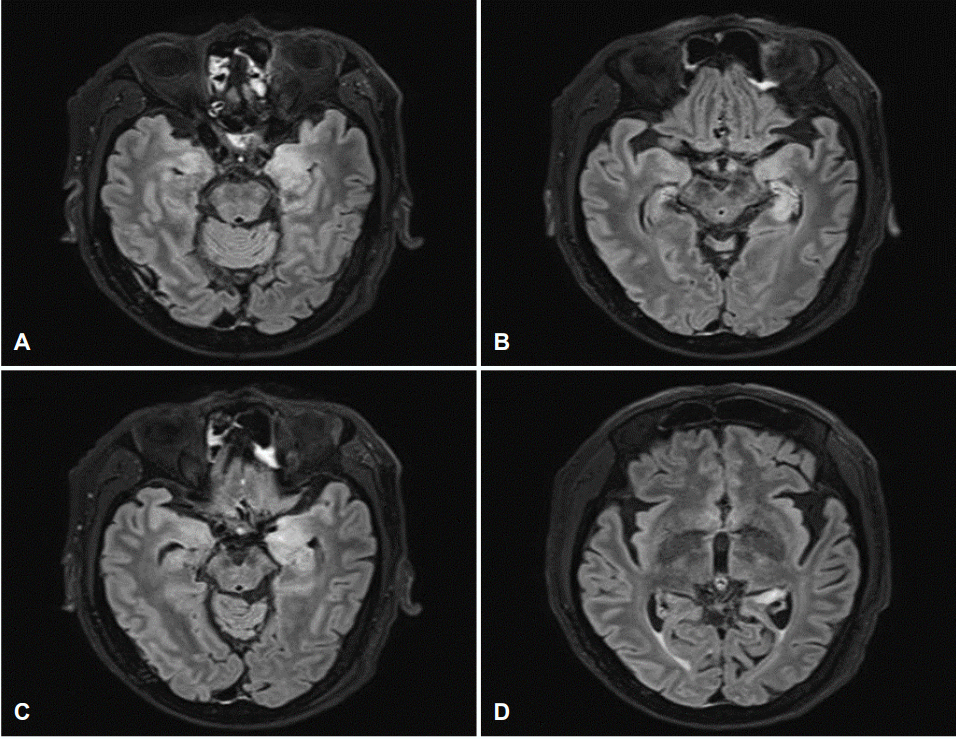
(A-D) Brain fluid attenuated inversion recovery (FLAIR) images show the bilateral medial temporal lobe including amygdala and hippocampus (especially worse on the left side).
환자의 흉부 computed tomography (CT) 소견에서 좌상엽에 결핵이 의심되는 결절성 폐병변, 우상엽에 9 mm 크기의 제자리 폐선암(adenocarcinoma in situ, AIS) 또는 최소침습폐선암(minimally invasive adenocarcinoma, MIA) 의심 병변이 있었는데 2번째 입원 당시 재검한 흉부 CT에서 좌상엽 결절 병변의 크기가 커져서 이에 대하여 절제술을 시행하였으며 병리검사 결과 폐결핵이 확진되어 이에 대하여 투약하였다. 폐결핵 확진 전까지 임상적으로 폐결핵을 의심할 증상 및 징후는 거의 없었다. 폐 우상엽에 보였던 제자리 폐선암/최소침습 폐선암 의심 병변은 3개월마다 흉부 CT를 재검하면서 병변의 크기가 커지면 수술 예정이다.
환자는 6개월 후 첫 경련이 발생하였으며 임상 양상은 전신강직간대발작(generalized tonic clonic seizure)이었으며 레비티라세탐(levitiracetam) 500 mg bid를 시작하였다. 7개월 후, 환자는 3번째 입원 후 퇴원하였고 퇴원 당시 기억력장애 외에는 특별한 신경계 이상은 없었다. 퇴원 전 시행한 마지막 혈액화학검사에서 Na 135 mg/dL로 정상 소견을 보였다. 환자는 퇴원 다음 날부터 1-2차례 경련을 하기 시작하였다. 보호자에 따르면 병원에 있을 때보다 엄청나게 많은 양의 물을 먹었다고 한다. 퇴원 2일 후에는 간헐적인 경련과 함께 보행이 불가능해지고 의식이 쳐지는 양상을 보였다고 한다. 이러한 증상 악화로 응급실에 내원하였고 내원 당시 혈액화학검사에서 Na 121 mg/dL로 저나트륨혈증을 보였다. 입원 당시 뇌파 소견은 전반적인 서파(continuous generalized theta-delta activity)를 보였다. 입원 후 3% NaCl 주사와 발프로산 450 mg bid 처방을 하였으며, 그 이후 발작 발생이 멈추고 의식이 정상으로 회복되었으며 정상적인 보행이 가능한 상태로 호전되었다.
입원 중 1차례 발작이 있었으며 당시 저나트륨혈증을 보였다(Fig. 1). 환자는 현재 심한 기억력저하를 보이는 CDR 1단계의 치매 상태로 유지 중에 있다.
고 찰
저자들은 질환 초기에 인지기능의 저하와 경련이 동반되지 않는 저나트륨혈증을 보였고, 면역글로불린, rituximab 그리고 tocilizumab과 같이 면역억제제를 사용한 투약 시기에는 저나트륨혈증이 없다가 치료 중단 이후 심해진 저나트륨혈증과 이에 따른 간질의 악화를 보인 증례를 경험하였기에 이를 보고한다.
항LGI-1항체뇌염에서 SIADH에 의한 발작의 악화에 대하여 최근 여러 보고들이 있다[5]. 본 증례는 퇴원 이후 환자가 수분 섭취 제한을 안 하면서 과량의 수분을 섭취하여, 저나트륨혈증의 악화를 보였고 이에 따라 뇌전증 발작의 횟수가 증가한 경우로 사료된다. 환자는 해마 이환에 의한 심한 기억력저하가 있어서 방금 전 수분을 섭취하고도 기억을 못하고 지속적인 수분 섭취를 하였다고 한다. 항LGI-1항체뇌염에서 기억력장애 등 인지장애가 발작 증가에 영향을 줄 수 있다는 것을 보여준다. 본 증례에서 첫 발작은 전신강직간대발작으로 질환에 특징적인 안면상완근긴장발작(faciobrachial dystonic seizure, FBDS)이 아니었으며 기억력장애와 인지장애가 발생한 후 약 8개월 뒤에 첫 발작을 보였다. 안면상완근긴장발작(FBDS)은 6월 퇴원 이후 발작이 빈번히 발생하였을 때 처음으로 관찰되었으며, 수초간 오른쪽 얼굴을 찡그리고 오른손이 불수적으로 꼬이면서 움직이는 양상을 보였다. 퇴원 이후 보호자가 관찰한 것이므로 정확한 발작 횟수는 알 수가 없었으며 FBDS 외에 전신강직간대발작도 있었다고 한다.
항LGI-1항체뇌염에서 인지장애 발생 전에 FBDS을 보여 스테로이드 면역억제 치료로 질환의 호전을 보인 국내 증례[6]와 달리, 본 증례는 다양한 면역억제 치료에도 불구하고 인지장애의 뚜렷한 호전이 없었고, 면역억제 치료 중에는 뇌전증발작이 거의 발생하지 않다가 면역억제 치료를 중단한 퇴원 시기에 저나트륨혈증의 발생과 더불어 발작이 집중적으로 발생한 경우이다. 본 환자의 당뇨병, 스테로이드 투여시 당뇨의 악화, 폐결핵 약제 투약에 따른 azathioprine, cyclophosphamide 등 기타 면역억제제의 사용 제한 그리고 제자리 폐선암/최소침습 폐선암 의심 병변 등이 환자의 예후에 영향을 주었을 것으로 사료된다. 항NMDAR항체, 항AMPAR 항체 그리고 항GABABR 자가면역뇌염 환자의 50% 정도에서 암 발생과 연관성을 보이나 항LGI-1항체뇌염에서 암발생률이 5% 정도로 매우 낮다고 알려져 있다[1]. 그러나 항LGI-1항체뇌염 환자 36명에 대하여 종양분석(tumor analysis)을 한 연구에서는 흉선종(thymoma), 신경내분비췌장종양(neuroendocrine pancreas tumor), 복부상피종(abdominal methothelioma) 그리고 제자리 직장암(rectal carcinoma in situ)이 4명의 환자에서 발생하여 11% 정도의 암발생률을 보였다[2]. 본 증례에서 뚜렷한 인지장애의 호전은 없었으나 다양한 면역억제제의 사용 이후 인지장애의 악화도 없었다(Fig. 2).
본 증례는 항LGI-1항체뇌염 환자에서 저나트륨혈증이 뇌전증발작의 악화를 초래하며 철저한 수분 섭취 제한을 통하여 발작의 악화를 예방할 수 있다는 것을 보여준다.