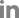| J Korean Neurol Assoc > Volume 35(3); 2017 > Article |
|
척-스트라우스증후군(Churg-Strauss syndrome, CSS)은 알레르기성 육아종혈관염으로 불리우는 천식과 같은 알레르기질환, 호산구증가증, 혈관염 및 혈관 외 조직에 육아종 형성을 특징으로 하는 전신혈관염의 하나이다[1]. CSS와 관련된 신경계 합병증으로는 다발단신경병증과 같은 말초신경질환이 약 65-75% 정도로 가장 흔하며 뇌경색 및 뇌출혈 등의 중추신경계와 연관된 합병증은 드물다[2]. CSS에서의 뇌경색은 작은 또는 중등도 크기의 혈관에 발생한 혈관염이나 심장내막의 호산구 침윤에 의한 심내막 섬유화로 인한 혈전색전증에 의해 발생한다고 추정되고 있다[2,3]. 실제로 CSS에서 발생하는 뇌경색의 양상은 다발성 또는 혈관의 분지 전체를 침범하는 경우가 대부분이다[2,3]. 본 저자들은 CSS 환자에서 단독으로 피질에만 국한된 뇌경색을 경험하여 이를 보고하고자 한다.
47세 남자가 컴퓨터 업무 중 갑작스럽게 발생한 좌측 상지의 근력 약화와 감각 이상 때문에 병원에 왔다. 환자는 과거력에서 27년 전 폐결핵을 진단받고 약물복용 후 완치 판정을 받았으며, 16년 전 천식 진단을 받았고 현재까지도 약물치료 중이었다. 또한 15년 전 비염과 부비동염으로 수술을 받았으며 그 당시 좌측 발바닥 및 우측 발등의 저린감과 통증이 동반되어 있어 타병원 신경과에서 CSS에 대한 검사를 받았다. 15년 전 타병원 검사 상 혈액검사에서 백혈구 9,140/mm3 (정상 4,000-10,000/mm3 )는 정상이었으나, 호산구의 개수가 3,840/mm3 (정상 50-500/mm3 ), 호산구의 분율이 42% (정상 0-5.8%)로 상승되어 있었다. C-반응성 단백질([0.241 mg/dL] [정상 0-0.3 mg/dL])과 류마티스인자([44.6 IU/mL [정상 0-18 IU/mL])도 상승되어 있었다. 항호중구세포질항체(antineutrophil cytoplasmic antibody, ANCA), 기생충검사, 대변잠혈반응 검사에서는 특이 소견이 없었다. 운동 및 감각신경전도검사 및 근전도검사는 정상이었으나 좌측 장딴지신경에서 신경생검 결과 축삭 변성이 확인되어 CSS로 진단받았다. 당시 고용량 스테로이드 치료를 5일간 시행 후 프레드니솔론(prednisolone 60 mg)과 사이클로포스파마이드(cyclophosphamide 50 mg)를 10년간 복용하다 증상의 재발 또는 악화가 없어 중단하였으며, 그 후에는 류코트리엔수용체 대항제인 몬테루카스트(montelukast sodium 10 mg)와 항히스타민제 레보세티리진(levocetirizine hydrochloride 5 mg) 등의 천식약만 복용하고 있었다.
본원에 좌측 상지의 MRC (medical research council) grade 4의 근력 약화와 우측 상지에 비해 10:7 정도의 통증과 온도감각 저하를 주소로 내원하였을 때 신체 활력징후는 혈압 134/89 mmHg, 호흡수 20회/분, 맥박수 91회/분, 체온 36.4℃였다. 양측 하지에서 심부건반사는 감소되었으며, 병적 반사는 음성이었다. 단순흉부방사선촬영에서 양측 하엽 부위에 관상의 음영증가 소견과 좌상엽에 이전 폐결핵 흔적이 남아 있었다(Fig. A). 이비인후과의 협의 진료에서 비염 및 부비동염이 확인되었다. 뇌자기공명영상 확산강조영상에서 우측 중심고랑 주변으로 전두엽과 두정엽의 대뇌피질에 고신호강도를 보여 급성 뇌경색에 합당하였다(Fig. B). T-1 조영증강 뇌자기공명영상에서 조영증강되는 병변은 관찰되지 않았으며 및 뇌자기공명 뇌혈관영상도 이상이 없었다. 혈액검사 상 호산구 14.3% (정상 0-5.8%), 면역글로불린E 1,115 IU/mL (정상 0-200 IU/mL), C-반응성 단백질 0.59 mg/dL (정상 0-0.3 mg/dL) 등이 상승되어 있었다. 또한 C단백, S단백, 프로트롬빈 시간, 활성화부분트롬보플라스틴 시간 및 자가면역질환 관련 혈액검사 상 d-이중체 0.88 mg/L (정상 0-0.59 mg/L), 피브리노젠 378.5 mg/dL (정상 180-350 mg/dL), 프로트롬빈 시간 14.0초(정상 10.7-13.8초), INR (international normalized ratio) 1.21(정상 0.9-1.15), 류마티스인자 20.8 IU/mL (정상 0-18 IU/mL) 등은 증가되거나 연장되어 있었다. 그 외 C형 및 P형 항호중구세포질항체, 항핵항체, 항이중나선항체, 한랭글로블린, 항카디오리핀항체, 루푸스 항응고인자를 비롯한 혈액검사결과는 모두 음성 또는 정상 범위였다. 심전도, 뇌졸중 집중치료실에서 48시간 동안 시행한 심장모니터링, 이후 24시간 동안의 홀터검사에서 이상이 없었으며 심장효소검사도 정상 범위였다. 내원 5일째 시행한 경흉부 및 식도경유심장초음파에서도 심장탓뇌경색의 원인이 확인되지 않았으며 심장 컴퓨터단층촬영(CT) 상 좌전하행지 원위부에서 40% 협착 소견이 관찰되었으나 그 외 심장 내에 혈전 및 대동맥에 동맥경화소견은 없었다.
환자는 본원 내원 당시부터 클로피도그렐(clopidogrel 75 mg) 및 아토르바스타틴(atorvastatin 40 mg)을 처방 받아 복용하였으며, 입원 5일째 환자의 근력저하는 MRC grade 5로 호전되었고 감각저하도 호전되어 퇴원하였으며 1년간의 추적 관찰 동안 재발은 없었다.
본 환자는 기존의 과거력(천식, 호산구증가증, 부비동염, 및 말초신경병증)과 본원 내원 당시의 천식의 병력, 10% 이상의 호산구 증가증, 부비동염, 폐침윤 등으로 미루어 미국류마티스학회에서 권고하는 CSS 진단 기준에 합당한 환자로 판단된다[4]. 또한 뇌경색의 원인 및 CSS의 심장 침범 등을 감별하기 위해 시행한 심전도 감시, 홀터검사, 경흉부 및 식도경유심장초음파, 심장 CT에서도 뇌경색의 원인이 되는 소견은 없었다. 따라서, CSS에 동반된 호산구 증가증에 의한 혈전색전증으로 뇌경색이 발생했을 가능성이 높다고 판단된다. 그러나 비록 호산구의 개수가 특발호산구증가증 진단 기준인 6개월 이상 지속되는 1.5×109 /L 이상의 호산구 증가에 해당하지는 않았으나[5], 호산구의 증감 여부를 추적 관찰하지 않았기 때문에 호산구증가증 자체로 발생한 뇌경색 가능성뿐만 아니라 원인 불명의 뇌경색일 가능성도 완전히 배제할 수는 없다.
현재까지, CSS에서 뇌경색이 동반된 경우는 드물게 보고되었다. 우리나라에서는 11년 동안 단일 기관에서 CSS으로 진단받은 16명의 환자의 신경학적 합병증을 조사하였을 때 이 중 3명에서 뇌경색이 발생하였다는 보고가 있다[2]. 이 3명 중 1명은 좌측 중뇌 동맥폐쇄가 동반된 뇌의 1/3이상의 뇌경색이 확인되었고, 다른 2명은 뇌혈관의 심한 협착은 관찰되지 않았으나 양측 대뇌 반구 여러 곳에 다발성의 뇌경색이 확인되었다[2]. 일본에서는 77세 여자 CSS 환자에서 발생한 우측 소뇌에 국한된 뇌경색을 보고한 바 있고[6], 유럽에서는 심방중격결손과 혈액응고인자 V R506Q 변이가 확인된 CSS환자에서 우측 기저핵에 출혈성 변환을 동반한 뇌경색을 보고한 바 있다[7]. 우리 증례의 경우, 단독으로 우측 대뇌 피질에 국한하여 뇌경색이 발생하였고 출혈성 변환을 동반하지 않았다는 점이 이전의 보고와 다르다.
결론적으로 본 증례는 CSS환자에서 다발성 또는 분지전체를 침범하지 않고 단독으로 피질에만 뇌경색이 생길 가능성도 있음을 주지시켜 준다.
Acknowledgements
This study provided financial support in the form of Basic Science Research Program through the National Research Foundation of Korea funded by the Ministry of Education (2015R1D1A1A01057934), grants of Korean Society of Neurosonology and Korean Neurological Association.
REFERENCES
1. Churg J, Strauss L. Allergic granulomatosis, allergic angiitis, and periarteritis nodosa. Am J Pathol 1951;27:277-301.


2. Kang DW, Jeong IK, Kim HJ, Lee KW. Neurologic manifestations of churg-Strauss syndrome. J Korean Neurol Assoc 1999;17:836-840.
3. Sehgal M, Swanson JW, DeRemee RA, Colby TV. Neurologic manifestations of churg-strauss syndrome. Mayo Clin Proc 1995;70:337-341.


Figure.
Chest X-ray and brain magnetic resonance images of patient. (A) Tubular opacities were observed in both lower lobes (arrowheads) and stable pulmonary tuberculosis was observed in the upper left lobe in patient’s chest X-ray. (B) Diffusion-weighted images showed high signal intensities in the right frontal and parietal cortex around the central sulcus (arrow).
- TOOLS
-
METRICS

-
- 0 Crossref
- 0 Scopus
- 6,815 View
- 72 Download
- Related articles
-
Memantine-induced Cortical Myoclonus in a Patient with Alzheimer’s Disease2023 November;41(4)
Multiple Cerebral infarction Associated with Heat Stroke2022 February;40(1)
Claw-Hand Caused by a Small Cortical Infarction in the Precentral Gyrus2018 August;36(3)
Acute Intestinal Pseudo-Obstruction in a Patient with MELAS Syndrome2017 November;35(4)



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print