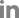2. Rizzi L, Rosset I, Roriz-Cruz M. Global epidemiology of dementia: Alzheimer's and vascular types.
Biomed Res Int 2014;2014:908-915.

4. Nygaard HB. Current and emerging therapies for Alzheimer's disease.
Clin Ther 2013;35:1480-1489.

5. Rogers SL, Farlow MR, Doody RS, Mohs R, Friedhoff LT. A 24-week, double-blind, placebo-controlled trial of donepezil in patients with Alzheimer’s disease. Donepezil study group.
Neurology 1998;50:136-145.

6. Cummings JL, Morstorf T, Zhong K. Alzheimer's disease drug-development pipeline: few candidates, frequent failures.
Alzheimers Res Ther 2014;6:37.

7. Jack CR Jr, Knopman DS, Weigand SD, Wiste HJ, Vemuri P, Lowe V, et al. An Operational approach to National Institute on Aging-Alzheimer's Association criteria for preclinical Alzheimer’s disease.
Ann Neurol 2012;71:765-775.



8. Sperling RA, Aisen PS, Beckett LA, Bennett DA, Craft S, Fagan AM, et al. Toward defining the preclinical stages of Alzheimer's disease: recommendations from the National Institute on Aging-Alzheimer's Association workgroups on diagnostic guidelines for Alzheimer's disease.
Alzheimers Dement 2011;7:280-292.

9. Albert MS, DeKosky ST, Dickson D, Dubis B, Feldman HH, Fox NC, et al. The diagnosis of mild cognitive impairment due to Alzheimer's disease: recommendations from the National Institute on Aging-Alzheimer's Association workgroups on diagnostic guidelines for Alzheimer's disease.
Alzheimers Dement 2011;7:270-279.

10. McKhann GM, Knopman DS, Chertkow H, Hyman BT, Jack CR Jr, Kawas CH, et al. The diagnosis of dementia due to Alzheimer's disease: recommendations from the National Institute on Aging-Alzheimer's Association workgroups on diagnostic guidelines for Alzheimer's disease.
Alzheimers Dement 2011;7:263-269.

11. Hardy J, Selkoe DJ. The amyloid hypothesis of Alzheimer's disease: progress and problems on the road to therapeutics.
Science 2002;297:353-356.

12. Jack CR Jr, Knopman DS, Jagust WJ, Shaw LM, Aisen PS, Weiner MW, et al. Hypothetical model of dynamic biomarkers of the Alzheimer's pathological cascade.
Lancet Neurol 2010;9:119-128.

13. Cummings JL. Defining and labeling disease-modifying treatments for Alzheimer’s disease.
Alzheimers Dement 2009;5:406-418.

14. Vellas B, Andrieu S, Sampaio C, Wilcock G. Disease-modifying trials in Alzheimer’s disease: a European task force consensus.
Lancet Neurol 2007;6:56-62.

15. Becker RE, Greig NH. Increasing the success rate for Alzheimer's disease drug discovery and development.
Expert Opin Drug Discov 2012;7:367-370.

16. Salloway S, Sperling R, Fox NC, Blennow K, Klunk W, Raskind M, et al. Two phase 3 trials of bapineuzumab in mild-to-moderate Alzheimer's disease.
N Engl J Med 2014;370:322-333.

17. Relkin N. Clinical trials of intravenous immunoglobulin for Alzheimer's disease. J Clin Immunol 2014;34(Suppl 1):S74-79.
18. Doody RS, Thomas RG, Farlow M, Iwatsubo T, Vellas B, Joffe S, et al. Phase 3 trials of solanezumab for mild-to-moderate Alzheimer's disease.
N Engl J Med 2014;370:311-321.

19. Mangialasche F, Solomon A, Winblad B, Mecocci P, Kivipelto M. Alzheimer's disease: clinical trials and drug development.
Lancet Neurol 2010;9:702-716.

20. Vellas B, Carrillo MC, Sampaio C, Brashear HR, Siemers E, Hampel H, et al. Designing drug trials for Alzheimer's disease: what we have learned from the release of the phase III antibody trials: a report from the EU/US/CTAD Task Force.
Alzheimers Dement 2013;9:438-444.

21. Vellas B, Sol O, Snyder PJ, Ousset PJ, Haddad R, Maurin M, et al. EHT0202 in Alzheimer's disease: a 3-month, randomized, placebo-controlled, double-blind study.
Curr Alzheimer Res 2011;8:203-212.

22. En Vivo Pharmaceuticals, Inc.. Safety, tolerability, pharmacokinetics of EVP-0962 and effects of EVP-0962 on cerebral spinal fluid amyloid concentrations in healthy subjects and in subjects with mild cognitive impairment or early Alzheimer's disease. Available from :
www.clinical trials.gov (Identifier: NCT01661673)..
23. Sabbagh MN, Agro A, Bell J, Aisen PS, Schweizer E, Galasko D. PF-04494700, an oral inhibitor of receptor for advanced glycation end products (RAGE), in Alzheimer disease.
Alzheimer Dis Assoc Disord 2011;25:206-212.

24. Panza F, Solfrizzi V, Imbimbo BP, Giannini M, Santamato A, Seripa D, et al. Efficacy and safety studies of gantenerumab in patients with Alzheimer's disease.
Expert Rev Neurother 2014;14:973-986.

26. Farlow MR, Andreasen N, Riviere ME, Vostiar I, Vitaliti A, Sovago J, et al. Long-term treatment with active Aβ immunotherapy with CAD106 in mild Alzheimer's disease. Alzheimers Res Ther 2015;7:23.
27. Katsuno M, Tanaka F, Sobue G. Perspectives on molecular targeted therapies and clinical trials for neurodegenerative diseases.
J Neurol Neurosurg Psychiatry 2012;83:329-335.

28. Administration US Department of Health and Human Services Food and Drug Administration.. Alzheimer's disease: Developing drugs for the treatment of early stage disease. 2013.
29. Gerald Z, Ockert W. Alzheimer's disease market: hope deferred.
Nat Rev Drug Discov 2013;12:19-20.

30. Zhang B, Carroll J, Trojanowski JQ, Yao Y, Iba M, Potuzak JS, et al. The microtubule-stabilizing agent, epothilone D, reduces axonal dysfunction, neurotoxicity, cognitive deficits, and Alzheimer-like pathology in an interventional study with aged tau transgenic mice.
J Neurosci 2012;32:3601-3611.

31. Ni R, Marutle A, Nordberg A. Modulation of α7 nicotinic acetylcholine receptor and fibrillar amyloid-β interactions in Alzheimer's disease brain. J Alzheimers Dis 2013;33:841-851.
32. Wilkinson D, Windfeld K, Colding-Jørgensen E. Safety and efficacy of idalopirdine, a 5-HT6 receptor antagonist, in patients with moderate Alzheimer's disease (LADDER): a randomised, double-blind, placebo-controlled phase 2 trial.
Lancet Neurol 2014;13:1092-1099.

33. Serrano-Pozo A, Vega GL, Lütjohann D, Locascio JJ, Tennis MK, Deng A, et al. Effects of simvastatin on cholesterol metabolism and Alzheimer disease biomarkers.
Alzheimer Dis Assoc Disord 2010;24:220-226.



34. He P, Cheng X, Staufenbiel M, Li R, Shen Y. Long-term treatment of thalidomide ameliorates amyloid-like pathology through inhibition of β-secretase in a mouse model of Alzheimer's disease. PLoS One 2013;8:e55091.
35. Claxton A, Baker LD, Hanson A, Trittschuh EH, Cholerton B, Morgan A, et al. Long-acting intranasal insulin detemir improves cognition for adults with mild cognitive impairment or early-stage Alzheimer's disease dementia. J Alzheimers Dis 2015;44:897-906.
36. Zhang RY, Leon AC, Chuang-Stein C, Romano SJ. A new proposal for randomized start design to investigate disease-modifying therapies for Alzheimer disease.
Clin Trials 2011;8:5-14.


37. Olanow CW, Rascol O, Hauser R, Feigin PD, Jankovic J, Lang A, et al. A double-blind, delayed-start trial of rasagiline in Parkinson's disease.
N Engl J Med 2009;361:1268-1278.

38. Moulder KL, Snider BJ, Mills SL, Buckles VD, Santacruz AM, Bateman RJ, et al. Dominantly Inherited Alzheimer Network: facilitating research and clinical trials.
Alzheimers Res Ther 2013;5:48-54.



39. Solomon A, Mangialasche F, Richard E, Andrieu S, Bennett DA, Breteler M, et al. Advances in the prevention of Alzheimer's disease and dementia.
J Intern Med 2014;275:229-250.

40. Sperling RA, Rentz DM, Johnson KA, Karlawish J, Donohue M, Salmon DP, et al. The A4 study: stopping AD before symptoms begin?
Sci Transl Med 2014;6:228-233.

41. Reiman EM, Langbaum JB, Fleisher AS, Caselli RJ, Chen K, Ayutyanont N, et al. Alzheimer’s Prevention Initiative: a plan to accelerate the evaluation of presymptomatic treatments. J Alzheimers Dis 2011;26(Suppl 3):321-329.
42. Kivipelto M, Solomon A, Ahtiluoto S, Ngandu T, Lehtisalo J, Antikainen R, et al. The finnish geriatric intervention study to prevent cognitive impairment and disability(FINGER): study design and progress.
Alzheimers Dement 2013;9:657-665.

43. Carrié I, van Kan GA, Gillette-Guyonnet S, Andrieu S, Dartigues JF, Touchon J, et al. Recruitment strategies for preventive trials. The MAPT study (MultiDomain Alzheimer Preventive Trial).
J Nutr Health Aging 2012;16:355-359.

44. Richard E, Van den Heuvel E, Moll van Charante EP, Achthoven L, Vermeulen M, Bindels PJ, et al. Prevention of dementia by intensive vascular care (PreDIVA): a cluster-randomized trial in progress.
Alzheimer Dis Assoc Disord 2009;23:198-204.





 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print